המומחה הרפואי של המאמר
פרסומים חדשים
תרופות
תרופות המונעות טרומבוז ומשפרות את הריאולוגיה של הדם
Last reviewed: 07.07.2025

כל תוכן iLive נבדק מבחינה רפואית או נבדק למעשה כדי להבטיח דיוק עובדתי רב ככל האפשר.
יש לנו קווים מנחים קפדניים המקור רק קישור לאתרים מדיה מכובד, מוסדות מחקר אקדמי, בכל עת אפשרי, עמיתים מבחינה רפואית מחקרים. שים לב שהמספרים בסוגריים ([1], [2] וכו ') הם קישורים הניתנים ללחיצה למחקרים אלה.
אם אתה סבור שתוכן כלשהו שלנו אינו מדויק, לא עדכני או מפוקפק אחרת, בחר אותו ולחץ על Ctrl + Enter.
במניעת היווצרות של מיקרותרומבוסים מרובים במהלך הלם והרסם, ניתן להשתמש בגישות פרמקולוגיות שונות המשתמשות בתרופות המונעות היווצרות תרומבוס ומשפרות את הריאולוגיה של הדם:
- חיסול הפרעות המודינמיות ומיקרו-סירקולציה מערכתיות באמצעות חומרים וזואקטיביים ואינוטרופיים;
- אמצעים לשיפור הריאולוגיה של הדם באמצעות טיפול עירוי רציונלי ותרופות המשקמות את גמישות קרומי כדוריות הדם האדומות (טרנטל או פנטוקסיפילן);
- מניעת הצטברות טסיות דם ויצירת תרומבי "לבנים" ראשוניים בכלי דם עורקיים קטנים ולאחר מכן תחילת מפל הקרישה;
- עיכוב היווצרות תרומבוס לאחר הפעלת מפל הקרישה הסיסטמי;
- הפעלת פיברינוליזה במטרה להמיס קרישי דם חדשים שנוצרו (פיברינוליזין, סטרפטוקינאז, סטרפטודקאז, אורוקינאז וכו') או, להיפך, עיכוב הפיברינוליזה כאשר היא מוכללת אצל חלק מהחולים עם הלם טראומטי וספסיס (חומצה אמינוקפרואית, אמבֶּן, קונטריקל וכו').
רוב הגישות המפורטות הן מסורתיות, מפותחות היטב בטיפול בהלם, בעלות אינדיקציות המורולוגיות משלהן והן מפורטות בפרקים הרלוונטיים. לכן, בסעיף זה מומלץ להתעכב על שיקול הגישה הכללית למניעת היווצרות פקקת בהלם באמצעות חומרים פרמקולוגיים המשפיעים על פרופאזה של קרישת הדם. רמת מניעת סיבוכי קרישה זו - הופעה, היווצרות וצמיחה של "פקקות עורקיות לבנות" - היא שמושכת את תשומת הלב הרבה ביותר של החוקרים.
הפרעות שונות ולעתים קרובות רב-כיווניות של קרישת דם עם הידרדרות הריאולוגיה שלה אופייניות לסוגים שונים של הלם. הסוג הספטי, האנדוטוקסיני, הכוויות, הטראומטיות והדימומיות המאפיין ביותר של הלם הוא היווצרות של מיקרותרומבי מרובים בכלי הדם הקטנים ביותר, הנגרמת על ידי הפרעות בהמודינמיקה מערכתית, הפרעות בכלי הדם והמיקרו-מחזור הדם, עיבוי דם, בוצה, ירידה בגמישות של קרומי כדוריות הדם האדומות, כמו גם גורמים כלליים ומקומיים רבים (אוטוקואידים) היוזמים שינויים מקומיים בהמוסטאזיס של קרישת דם והכללת פרופאזה של קרישת דם.
בצורה סכמטית (מקוצרת), מוצגים השלב הראשוני של קרישת הדם ומנגנון ההומאוסטזיס המקומי של קרישת הדם כדלקמן.
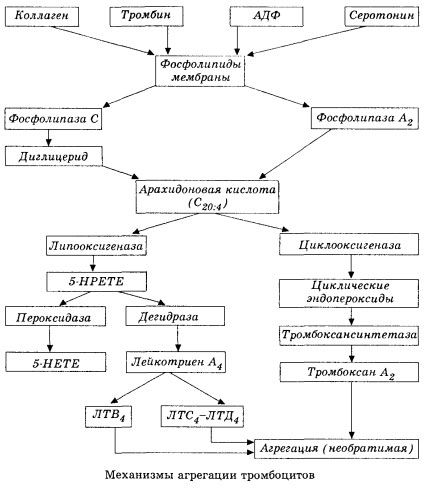
זה מתחיל בהפעלת פוספוליפאז A2 בממברנה כתוצאה מהשפעת שילוב של גורמים מזיקים (נזק ישיר לממברנה, היפוקסיה, חמצון שומנים, השפעת גורמים כימיים אנדוגניים וכו'). כתוצאה מפירוק פוספוליפידים בממברנה, משתחררות חומצות שומן ארוכות שרשרת לא אסטריות, שחומצה ארכידונית היא החשובה ביותר כסובסטרט התחלתי. הטרנספורמציה שלה (מפל חומצה ארכידונית) מתרחשת דרך מסלולי ליפוקסיגנאז (סינתזה של לויקוטריאנים) וציקלואוקסיגנאז (סינתזה של פרוסטגלנדינים, טרומבוקסנים, פרוסטציקלין).
הלויקוטריאנים הנוצרים (B4, C4, E4, D4 וכו') - חומרים בעלי פעילות ביולוגית גבוהה ביותר, הכוללים את החומר המגיב לאט של אנפילקסיס - הם בעלי חשיבות רבה בייזום תגובות מקומיות בכלי הדם, דלקתיות וחיסוניות, כולל תהליכים אוטואימוניים. לויקוטריאנים גורמים להפרעות במיקרו-סירקולציה, לקרישת דם מוגברת, לשחרור אנזימים ליזוזומלים אוטוליטיים ולשחרור לדם של גורם המעכב את התכווצות שריר הלב ועוויתות הסימפונות.
בשל יכולתם לגרום להתכווצות שרירים חלקים, לויקוטריאנים משפיעים באופן משמעותי על ההמודינמיקה המערכתית, כלי הדם הכליליים ושריר הלב, ומפעילים השפעה מכווץ כלילי חזקה ואפקט אינוטרופי שלילי, המלווה בירידה בתפוקת הלב וממלא תפקיד חשוב בהתפתחות לחץ דם נמוך.
תפוקת לב מופחתת ותגובה היפוטנסיבית ללויקוטריאנים קשורות להיחלשות שריר הלב ולהגבלת החזרה הוורידית ללב. חשיבות משמעותית בהגבלת החזרה הוורידית היא יכולתם של לויקוטריאנים להגביר את חדירות דופן כלי הדם ולגרום לפריקת פלזמה. לויקוטריאנים נחשבים חשובים בפתוגנזה של אוטם שריר הלב.
בהלם אנפילקטי וספטי (אנדוטוקסין), תפקידם ככל הנראה גובר עוד יותר, כפי שמעידה יכולתם של לויקוטריאנים להצטבר בכמויות משמעותיות בפלזמה במהלך תגובות אלרגיות ולגרום לשינויים בזרימת הדם המערכתית האופיינית להלם אנפילקטי, כמו גם ההשפעות המגנות של חוסמי קולטני לויקוטריאנים ומעכבי ליפוקסיגנאז. פיתוח חוסמי קולטני לויקוטריאנים סלקטיביים מתבצע באופן אינטנסיבי למדי ומהווה כיוון מבטיח של המדע. בתחום זה כבר הושגה הצלחה מסוימת ויעילותם של חוסמים כאלה באיסכמיה של שריר הלב, אנדוטוקסין והלם דימומי אושרה בניסוי. עם זאת, סביר להניח שיחלפו עוד מספר שנים עד שכיוון זה ייושם קלינית.
אם בכלי דם ורידיים נוצרים תרומבי בהשתתפות שווה של תרומבוציטים וגורמי קרישה בפלזמה, אז בעורקים תרומבוציטים הם היוזמים העיקריים של התהליך. הם מכילים ADP, Ca2+, סרוטונין, פוספוליפידים, אנזימים של סינתזת פרוסטגלנדינים ותרומבוקסן, תרומבוסטנין (כמו אקטומיוזין שריר מספק יכולת התכווצות של תאים אלה), גורם גדילה טרומבוגני של תאי אפיתל ושריר של דופן כלי הדם ומספר חומרים אחרים. ויסות הומורלי של תפקודי תרומבוציטים מתבצע באמצעות קולטנים מיוחדים של הממברנות שלהם (רצפטורים אלפא 2 ו-beta 2 אדרנרגיים, קולטנים להיסטמין וסרוטונין, אצטילכולין, תרומבוקסן, אדנוזין ועוד מספר). תכונה מיוחדת של תרומבוציטים היא זיקה גבוהה לקולגן ולאלמנטים תת-אנדותליאליים אחרים של דופן כלי הדם, למשטחים שאינם מרטיבים ומטעונים שלילית. תכונה זו מספקת לתרומבוציטים יכולת יוצאת דופן להידבק (להיצמד) לחלק של כלי דם עם אנדותל פגום, שיש לו הזדמנות רבה להינזק במהלך הלם. במקרה זה, תרומבוציטים מתפשטים ומשחררים פסאודופודיה, אשר יכולים להידבק זה לזה ולדופן כלי הדם. חדירות הממברנה עולה, ו-ADP, סרוטונין, תרומבוקסאן וכמה גורמי קרישה הנספחים על פני השטח של התרומבוציטים משתחררים מהתרומבוציטים. חומרים אלה מקיימים אינטראקציה עם הקולטנים המתאימים על הממברנה, ובהשתתפות יוני סידן, גורמים לאגרגציה (בתחילה הפיכה). התהליך הופך לעצמו, דבר שמקל על ידי גורמים רגולטוריים הומורליים; גורמים אחרים, לעומת זאת, יכולים לעצור אותו ואף להפוך אותו, ולגרום לפירוק.
עם דומיננטיות של השפעות ותנאים יוצרי פקקת, שלבי ההידבקות והצבירה ההפיכים מוחלפים בשלב השלישי - צבירה בלתי הפיכה, המתבצעת בהשתתפות תרומבוסטנין ומוביל להיצרות הקריש; תגובת חיזוק הצבירה וההיצרות מתרחשת גם בהשתתפות Ca +, ATP ומובילה להיווצרות פקקת לבנה.
מסלול הציקלואוקסיגנאז של המרת חומצה ארכידונית בטסיות דם, תאי אנדותל כלי דם ורקמות אחרות מבטיח הומאוסטזיס מקומי (זמן מחצית החיים של מטבוליטים קצר מאוד), מכיוון שבמהלך מטבוליזם זה נוצרים חומרים מעודדי ונוגדי-אגרגמנטים רבי עוצמה. הגורם העיקרי המפעיל את צבירת הטסיות בשרשרת התגובות של ציקלואוקסיגנאז הוא טרומבוקסאן A2, והאנטגוניסט החזק לא פחות שלו הוא פרוסטציקלין, המיוצר על ידי תאי אנדותל, ובמידה פחותה, פרוסטגלנדינים מסדרות E ו-G. לבסוף, צבירת טסיות מושפעת מאוד מגורמים הומורליים מקומיים ומערכתיים נוספים.
מפעילי ומעכבי צבירת טסיות דם
יוזמים ומפעילים של צבירת טסיות דם |
מעכבי צבירת טסיות דם |
קולגן |
- |
ADP |
אדנוזין ומייצבים שלו |
נוראפינפרין (דרך קולטני אלפא 2) |
חומרים חוסמי אלפא-אדרנרגיים |
סרוטונין |
חומרים אנטי-סרוטונין |
היסטמין |
אנטי-היסטמינים |
טרומבין |
הפרין |
סידן2+ |
אנטגוניסטים של Ca2+ |
CGMP - המעוררים שלו (אצטילכולין?) והמייצבים שלו |
CAM - המעוררים שלו (דרך קולטנים בטא-אדרנרגיים) והמייצבים שלו (מעכבי פוספודיאסטראז) |
חומצה ארכידונית |
דקסטרנים, אלבומין |
תרומבוקסאן A2 |
פרוסטציקלין I2 |
התערבויות פרמקולוגיות בשלב הראשוני של היווצרות פקקת בהלם ובתהליכים איסכמיים חריפים בלב ובמוח מצביעות על האפשרות הבאה:
- עיכוב של תגובות ראשוניות (מוחלטות וחלקיות) של מפל חומצה ארכידונית;
- עיכוב של תגובה מסוימת של סינתזת טרומבוקסאן;
- חסימת קולטנים ללויקוטריאנים ותרומבוקסנים בטסיות דם, שריר חלק ותאים אחרים;
- שימוש בחומרים המווסתים את צבירת טסיות הדם, כלומר מחלישים בדרכים אחרות את תגובתן להשפעת גורמים מקדמים (קולגן, טרומבוקסאן A2, לויקוטריאנים וכו').
יישום הדרכים המפורטות לתיקון הפרעות בתכונות הריאולוגיות של הדם מספק פתרון למשימה הטקטית העיקרית: הגנה על קולטני הצבירה וההידבקות של טסיות דם מהשפעת מפעילים או דיכוי מנגנונים תוך תאיים של סינתזה של קולטנים אלה. עיכוב התגובות הראשוניות של מפל חומצה ארכידונית יכול להיות מושג על ידי הגנה על קולטני טסיות דם המגיבים למפעילי פולימרים, באמצעות דקסטרנים בעלי מולקולות נמוכות, שמולקולותיהם מתחרות עם פיברין, קולגן, אימונוגלובולין מצטבר (IgE) ורכיבים של מערכת המשלים.
על ידי הסתרת הקולטנים על קרום הטסיות ותחרות עם חלבונים מפוזרים בגודל על פני השטח של אריתרוציטים, דקסטרנים בעלי מולקולות נמוכות דוחקים אותם והורסים את הגשרים בין התאים. זאת בשל העובדה שדקסטרנים, העוטפים את האנדותל של כלי הדם ואת פני השטח של יסודות תאי הדם, מגבירים את המטען השלילי שלהם, ובכך משפרים את תכונות נוגדות הצטברות.
דקסטרנס
דקסטרנים בעלי משקל מולקולרי נמוך מפחיתים את הצטברות הטסיות המושרה על ידי קולגן ו-ADP, כמו גם את ההשפעה המפעילה של תרומבין על טסיות הדם, מעכבים את צמיחת הפקקת הראשונית של טסיות הלבנות, משפרים את זרימת הדם, מפחיתים את העלייה בתכולת הפיברינוגן בפלזמה לאחר הניתוח ומשנים את המבנה והיציבות של הפיברין.
עירויים תוך-ורידיים של דקסטרנים בטראומה ובהלם לא רק מפחיתים את הצטברות הטסיות וההידבקות שלהן, אלא גם מגייסים הפרין אנדוגני, ובכך מקדמים היווצרות של קריש דם רופף וניתן לשליפה קשה, אשר מתפרק בקלות על ידי חומרים פיברינוליטיים. פעילות האנטי-תרומבין של דקסטרנים בעלי מולקולות נמוכות קשורה להשפעתם הספציפית על המבנה והתפקוד של גורם קרישת הדם VIII. פקטור VIII (גלובולין אנטי-המופילי), מולקולה גדולה בעלת מבנה ותפקוד מורכבים, מעורב בצבירת טסיות דם וביציבות הקריש שנוצר. דקסטרנים מפריעים לפעולתו של פקטור VIII, ובכך מאטים את צבירת הטסיות ומפחיתים את יציבות הקריש.
דקסטרנים בעלי משקל מולקולרי נמוך אינם נוגדי קרישה אמיתיים והשפעתם המתקנת בהפרעות דימויות קשורה בעיקר לדילול דם, חידוש נפח הפלזמה במחזור הדם ושיפור זרימת הדם במערכת המיקרו-סירקולציה.
יכולתם של דקסטרנים לשפר את זרימת הדם בהפרעות המודינמיות (הלם, איבוד דם) נובעת ממכלול של גורמים. הופעת ריכוז חולף גבוה של הפולימר בדם לא רק מובילה ל"דילול דם ישיר", אלא גם יוצרת תנאים לזרימת נוזלים לזרם הדם מהחלל הבין-ממדי ולאיזון שלאחר מכן של ההשפעה האוסמוטית של הדקסטרן. כתוצאה מהדילול המודי, צמיגות הדם יורדת, הזרימה הוורידית ללב עולה ותפוקת הלב עולה. יחד עם השפעות אלו, דקסטרנים יוצרים קומפלקסים עם פיברינוגן ויש להם השפעה נוגדת שומנים.
לפיכך, פעולת האנטי-אגרגציה וההשפעות ההמודינמיות של דקסטרנים בעלי ריכוז מולקולרי נמוך מסייעות להפחית את צמיגות הדם, דבר שחשוב במיוחד בקצבי גזירה נמוכים. פירוק תאי הדם משפר את זרימת הדם הסיסטמית ואת המיקרו-סירקולציה, במיוחד בחלק הוורידי שלה, שם גרדיאנטי המהירות הם הנמוכים ביותר. השימוש בתמיסות דקסטרן בעלות ריכוז מולקולרי נמוך בסוגים שונים של הלם, במהלך טיפול כירורגי בפציעות והשלכותיהן, ולאחר מכן בתקופה שלאחר הניתוח מסייע במניעת היפר-קרישה ולהפחית את הסבירות לתהליכים טרומבוטיים ותסחיף.
עם זאת, יש לציין שבמקרים מסוימים, עירויים של תמיסות דקסטרן מלווים בתגובות אנפילקטיות ואלרגיות (מסוכנות בנוכחות רגישות והלם אנפילקטי). זאת בשל העובדה שדקסטרנים, בעלי משקל מולקולרי גבוה ושרשראות צד רבות, יכולים לשמש כאנטיגן. לכן, כדי לקבוע רגישות אישית, מומלץ לתת מראש דרך הווריד עד 20 מ"ל של תמיסת דקסטרן דלת מולקולות כהפטן (תמיסה 15%, משקל מולקולרי 1000) ולבצע עירויים של תחליף פלזמה לפני הכנסת הרדמה.
 [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ]
[ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ]
מעכבי תרומבין
הגנה פרמקולוגית על קולטני טסיות דם המקיימים אינטראקציה עם מפעילי טסיות דם יכולה להיות מושגת גם באמצעות חומרים המתחרים במפעילי טסיות דם לא פולימריים או מעכבים אותם. חומרים כאלה כוללים מעכבי תרומבין (הפרין והירודין, מספר מעכבים סינתטיים, אנטגוניסטים לאדרנלין), חוסמי קולטני אלפא (פנטולאמין, דיהידרו-ארגוטמין), אנטגוניסטים ל-ADP (דיפירידמול, אדנוזין והאנלוגים המבניים שלו, פוספוקריטין), אנטגוניסטים לסרוטונין (מתיסרגיד). רק מעטים מהחומרים המפורטים משמשים בפועל למניעה וטיפול בהלם ממקורות שונים.
הגנה על מנגנונים תוך תאיים של סינתזה של קולטני חלבון המגיבים עם מפעילי צבירה והידבקות טסיות דם, ועיכוב תהליכי סינתזת טרומבוקסאן אפשריים עם תרופות מקבוצות שונות:
- מעוררים ומייצבים של cATP, פרוסטציקלין ופרוסטגלנדין PgE2;
- מעכבי פוספוליפאז ופוספודיאסטראז.
פיתוח אינטנסיבי של חומרים מיוחדים נוגדי טסיות החל יחסית לאחרונה ועדיין לא הוביל לתוצאות אמינות. כיום, בפרקטיקה הקלינית, בנוסף לתמיסות דקסטרן, נעשה שימוש נרחב בתרופות נוגדות טסיות כגון חומצה אצטילסליצילית, אינדומטצין, דיפיראדמול, סולפינפירזון (פרסנטין), פרוסטציקלין (איקופרוסטנון) והפרין כדי למנוע היווצרות של טרומבוסים לבנים בטסיות דם.
תרופות נוגדות דלקת לא סטרואידיות
נקבע כי ההשפעות הפרמקולוגיות של תרופות נוגדות דלקת שאינן סטרואידיות - חומצה אצטילסליצילית ואינדומטצין - נובעות מהשפעתן על חילוף החומרים של איקוסנואידים (תרומבוקסנים ופרוסטגלנדינים). כמעט כל התרופות בקבוצה זו מעכבות את קומפלקס האנזים המכונה סינתטאז פרוסטגלנדין, ובכך מפעילות את ההשפעות הספציפיות והאנטי-אגרגמנטיות שלהן.
חומצה אצטילסליצילית נספגת מהר מאוד לאחר מתן דרך הפה. תוצר ההידרוליזה שלה, חומצה סליצילית, גורם לעיכוב של ציקלואוקסיגנאז טסיות דם, אשר משבש את ההמרה של חומצה ארכידונית לפרוסטגלנדין O2 ובסופו של דבר, לטרומבוקסאן A2. חומצה אצטילסליצילית מעכבת צבירה הנגרמת על ידי קולגן, ADP, אדרנלין וסרוטונין. למרות ש-GG05 שלה הוא 15 דקות, ההשפעה נוגדת הצבירה נמשכת מספר ימים, דבר המוסבר ככל הנראה על ידי עיכוב בלתי הפיך של תגובות סינתזת פרוסטגלנדין ודיכוי תפקוד צבירה של טסיות דם לאורך כל חייהן (6-10 ימים). יחד עם עיכוב של ציקלואוקסיגנאז טסיות דם, חומצה אצטילסליצילית במינונים גבוהים מעכבת ציקלואוקסיגנאז של דופן כלי הדם, ובמקביל לדיכוי סינתזת טרומבוקסאן A2 מעכבת סינתזת פרוסטציקלין בתאי אנדותל. לכן, יש לרשום חומצה אצטילסליצילית כנוגדת צבירה במינונים קטנים (3000-5000 מ"ג/יום), אשר מעכבים בעיקר צבירה של טסיות דם.
בהתחשב בכך שחומצה אצטילסליצילית חוסמת את ציקלואוקסיגנאז טסיות במשך מספר ימים, ואת ציקלואוקסיגנאז האנדותל - לא יותר מיום, רציונלי לרשום את התרופה לא מדי יום, אלא כל 3-4 ימים. בחירת המינון האופטימלי של חומצה אצטילסליצילית עבור המטופל צריכה להתבצע באופן פרטני, מכיוון שיש רגישות שונה של המטופלים להשפעה נוגדת הטסיות של התרופה. בחולים תגובתיים, חומצה אצטילסליצילית במינון של 0.5 גרם מעכבת את צבירת הטסיות ב-40-50%, בחולים היפר-תגובתיים - לחלוטין או ב-80-90%, ובחולים תגובתיים, היעדר השפעה נוגדת טסיות מאופיין בעת נטילת אותה מינון של התרופה.
מעכבי סינתטאז טרומבוקסאן סלקטיביים הם אימידאזול והאנלוגים שלו, שאינם חוסמים את ציקלואוקסיגנאז. דיפירידמול, המשמש בפועל קליני לטיפול במחלת לב איסכמית כרונית כמרחיב כלילי, כמו אימידאזול, מעכב באופן סלקטיבי את סינתטאז טרומבוקסאן, ומונע את הסינתזה של טרומבוקסאן A2. התרופה והאנלוגים שלה נחשבים כמעכבים גם את פוספודיאסטראז טסיות הדם, ובכך מגדילים את ריכוז ה-cAMP בטסיות הדם. יחד עם זאת, דיפירידמול מעכב את פעילות אדנוזין דאמינאז ואת ספיגת אדנוזין על ידי טסיות הדם, חוסם את ספיגת הסרוטונין על ידי טסיות הדם ואת הצבירה שלהן הנגרמת על ידי אדרנלין וקולגן. ישנם דיווחים על פעילות נוגדת טסיות חלשה של התרופה ויכולתה במינונים קטנים לשפר את הצבירה של טסיות הדם. ניתן להשיג את ההשפעה נוגדת הטסיות האמינה ביותר באמצעות שילוב של דיפירידמול וחומצה אצטילסליצילית.
הפרין
מבין חומרים נוגדי תרומבוזיס, אחד המווסתים היעילים ביותר של מצב הצבירה של הדם הוא הפרין, במיוחד כאשר משתמשים בו בשלב מוקדם. להפרין מטען שלילי גבוה והוא מסוגל לתקשר עם יונים ומולקולות גדולים וקטנים כאחד (אנזימים, הורמונים, אמינים ביוגניים, חלבוני פלזמה וכו'), כך שספקטרום הפעולה הביולוגית שלו רחב למדי. לתרופה יש השפעות אנטי-תרומבין, אנטי-תרומבופלסטין ואנטי-פרותרומבין, מונעת את ההמרה של פיברינוגן לפיברין, מדכאת נסיגת קריש דם ומגבירה את הפיברינוליזה.
מנגנון הפעולה נוגדת הקרישה של הפרין הוא מורכב למדי. כיום נקבע כי ההשפעות נוגדות הקרישה של הפרין קשורות להגברת פעולת האנטי-תרומבין III ולשיפור יכולתו של קומפלקס הפרין-אנטי-תרומבין III להשבית במהירות את רוב פרוטאזות הסרין של מערכת קרישת הדם. בהשפעה נוגדת הקרישה של הפרין, ליכולתו להגדיל ולשמור על פוטנציאל אלקטרושלילי גבוה של האינטימה של כלי הדם, למנוע הידבקות טסיות דם ולהיווצרות מיקרו-תרומבוסים של טסיות דם, יש חשיבות רבה. הפרין מדכא באופן הפעיל ביותר היווצרות תרומבוס בוורידים, ומונע הן היווצרות תרומבוס מקומית והן קרישה תוך-וסקולרית מפושטת.
פרוסטציקלין והאנלוגים היציבים שלו
מבין חומרים נוגדי טסיות דם, מעכבי הצבירה החזקים ביותר הם פרוסטציקלין והאנלוגים היציבים שלו. ההשפעה נוגדת הטסיות של פרוסטציקלין נובעת מגירוי של אדנילט ציקלאז וכתוצאה מכך, עלייה בריכוז cAMP בטסיות דם, ירידה בתכולת התרומבוקסאן, ירידה בתכולת התרומבוקסאן A2 וחסימת קולטניו. פרוסטציקלין אינו יציב ומתפרק במהירות לתוצרים לא פעילים, ולכן הוא מנוהל תוך ורידי בטפטוף בקצב של 2 עד 20 ננוגרם/ק"ג לדקה למשך 30-60 דקות עד 6 פעמים ביום.
לפרוסטציקלין, יחד עם השפעה נוגדת צבירה חזקה, יש השפעה מרחיבה כלי דם וסמפונות חזקה. התרופה מרחיבה את כלי הדם של המוח, הלב, הכליות, שרירי השלד וכלי הדם המזנטריים. תחת השפעת הפרוסטציקלין, זרימת הדם הכליליים עולה, אספקת האנרגיה של שריר הלב עולה והצורך שלו בחמצן פוחת. למרות חוסר היציבות שלו בגוף, השפעות חיוביות קליניות יכולות להימשך מספר שבועות ואף חודשים. מנגנון הפעולה הממושכת הזו עדיין אינו ברור.
פרוסטציקלין היא תרופה בעלת רעילות נמוכה, אך השימוש בה עלול לגרום לתופעות לוואי: אדמומיות בפנים, כאבי ראש, ירידה בלחץ הדם, כאבי בטן, אנורקסיה. יחד עם פרוסטציקלין, האנלוגים הסינתטיים היציבים שלה (אילופרוסט וכו') הם מעכבים מבטיחים של צבירת טסיות דם.
תרופות המשפרות את צמיגות הדם
הפרעות בתכונות הריאולוגיות של הדם במהלך טראומה והלם נגרמות לא רק משינויים בפעילות התפקודית של טסיות הדם, אלא גם מעלייה בצמיגות הדם. הצמיגות המבנית של הדם כמערכת דינמית מורכבת ומפוזרת נקבעת במידה רבה על ידי צמיגות הפלזמה ויכולתם של אריתרוציטים להתעוות. צמיגות הפלזמה תלויה בעיקר בריכוז החלבונים בדם. חלבונים בעלי משקל מולקולרי קטן, כגון אלבומין, משפיעים מעט על צמיגות הפלזמה, בעוד שחלבונים בעלי מולקולה גדולה (פיברינוגן, אלפא וגמא גלובולינים, מקרומולקולות אחרות) מגדילים אותה משמעותית.
בקצבי גזירה נמוכים, ספיחה של פיברינוגן וגלובולינים על פני השטח של אריתרוציטים מובילה ליצירת גשרים בין תאים סמוכים וליצירת צברים מהאריתרוציטים. קצב היווצרות הצברים הוא תהליך ביופיזיקלי מורכב ותלוי לא רק בגודל הגזירה, אלא גם בתכונות האלקטרוקינטיות של אריתרוציטים, בריכוז, במסה וביכולת הספיחה של המקרומולקולות-צברות, ובצורה ובפלסטיות של אריתרוציטים.
שמירה על הצורה והתכונות המכניות של קרום כדוריות הדם האדומות דורשת הוצאת אנרגיה משמעותית. ההנחה היא שהאנרגיה המופקת בכדוריות הדם האדומות במהלך הגליקוליזה מושקעת בזרחון של ספקטרין, מה שמביא לשינויים במבנה המשני של החלבון ולאינטראקציה עם רכיבים שכנים של הממברנה הפנימית. האינטראקציה בין החלבונים המבניים של הממברנה, ספקטרין ואקטין, ממלאת תפקיד חשוב ביצירת התכונות המכניות של קרום כדוריות הדם האדומות, בשמירה על שטח פנים קבוע של כדוריות הדם האדומות ועובין תחת כל עיוות.
במקרה של הפרעות סיסטמיות בזרימת הדם של האדים האדומים ואיברים, העלייה בקשיחות קרומי האדומים האדומים והיווצרות צבירי אדומים מובילים לירידה בקצב המעבר של האדומים האדומים דרך נימים, ובכך משבשים את תפקוד הובלת הגזים של הדם. לכן, תיקון הפרעות בתכונות הריאולוגיות של הדם בהלם צריך לכלול, יחד עם מניעת צבירת אדומים אדומים, נרמול של צמיגות הפלזמה והדם, צבירתם ועיוותם של האדומים האדומים.
בנוסף לדקסטרנים בעלי מולקולות נמוכות, תמיסות אלבומין הן אחד האמצעים היעילים להגברת יציבות הדם בתרחיף. בתקופה המאוחרת של הלם, מתרחשת הצטברות כללית של אריתרוציטים על רקע ירידה בריכוז האלבומין בפלזמת הדם ועלייה בריכוז הפיברינוגן והגלובולינים, במיוחד מקטע אלפא 2, ליפופרוטאינים וליפידים. בתנאים אלה, ההשפעות הריאולוגיות של אלבומין נובעות משני גורמים עיקריים: דילול דם ונורמליזציה של היחס בין חלבונים מיקרו-מקרוגלובולריים בפלזמה. במקביל, אלבומין נקשר לחומצות חופשיות, שתייצובן במהלך טראומה והלם מגרה את הצטברות המבנים התאיים של הדם ואת קרישת הדם התוך-וסקולרית ויכול לגרום לתסחיף שומן.
אמצעים נגד הלם שמטרתם לחדש את נפח הדם במחזור הדם, למנוע היפוקסיה ברקמות וחמצת מטבולית, תורמים לנרמול האלסטיות של קרומי האדומים, שכן היפוקסיה וחמצת מפחיתות משמעותית את יכולת העיוות של האדומים. קשיחות מוגברת של קרומי האדומים בהלם קשורה כנראה לעיכוב סינתזת ATP באדומים. בתורו, ירידה בריכוז ה-ATP תורמת לעלייה בריכוז ה-Ca2+ באדומים, אשר, על ידי קשירה לחלבוני הממברנה, מגבירים את קשיחות הממברנה.
אחת התרופות הפרמקולוגיות המגבירות את תכולת ה-ATP באדומים תאי הדם ואת גמישות קרומי האדומים תאי הדם היא טרנטל (פנטוקסיפילין), המשמשת בפועל קליני לטיפול בהפרעות איסכמיות.
יחד עם הפחתת נוקשות קרומי כדוריות הדם האדומות, טרנטאל גורם להרחבת כלי דם, משפר את חמצון הרקמות, מעכב את פעילות פוספודיאסטראז ברקמות, מגביר את ריכוז ה-cAMP ומעכב צבירת טסיות דם.
בין שאר החומרים הפרמקולוגיים השומרים על גמישות קרום כדוריות הדם האדומות, ראוי לציין אנטגוניסטים של Ca2+, אשר מגבילים את זרימת היונים לתוך כדוריות הדם האדומות (פלונריזין, ניפדיפין וכו').
 [ 19 ], [ 20 ], [ 21 ], [ 22 ], [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ]
[ 19 ], [ 20 ], [ 21 ], [ 22 ], [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ]
תשומת הלב!
כדי לפשט את תפיסת המידע, הוראה זו לשימוש בתרופה "תרופות המונעות טרומבוז ומשפרות את הריאולוגיה של הדם" מתורגמת ומוצגת בצורה מיוחדת על בסיס ההנחיות הרשמיות לשימוש רפואי של התרופה. לפני השימוש קרא את ההערה כי הגיע ישירות לתרופה.
תיאור מסופק למטרות מידע אינו מדריך לריפוי עצמי. הצורך בתרופה זו, מטרת הטיפול, השיטות והמנה של התרופה נקבעת אך ורק על ידי הרופא המטפל. תרופה עצמית מסוכנת לבריאות שלך.

