המומחה הרפואי של המאמר
פרסומים חדשים
שסתומי לב
סקירה אחרונה: 23.04.2024

כל תוכן iLive נבדק מבחינה רפואית או נבדק למעשה כדי להבטיח דיוק עובדתי רב ככל האפשר.
יש לנו קווים מנחים קפדניים המקור רק קישור לאתרים מדיה מכובד, מוסדות מחקר אקדמי, בכל עת אפשרי, עמיתים מבחינה רפואית מחקרים. שים לב שהמספרים בסוגריים ([1], [2] וכו ') הם קישורים הניתנים ללחיצה למחקרים אלה.
אם אתה סבור שתוכן כלשהו שלנו אינו מדויק, לא עדכני או מפוקפק אחרת, בחר אותו ולחץ על Ctrl + Enter.
מוקדם יותר היה חושב כי כל שסתומי הלב הם מבנים פשוטים אשר תרומתו זרימת הדם חד כיווני הוא פשוט תנועה פסיבית בתגובה מדרון הלחץ משחק. הבנה זו של "מבנים פסיביים" הובילה ליצירתם של תחליפי שסתומים מכניים וביולוגיים "פסיביים".
עכשיו מתברר כי שסתומי הלב יש מבנה מורכב יותר לתפקד. לפיכך, יצירת תחליף שסתום הלב "הפעיל" מצביע על דמיון משמעותי במבנהו ובפונקציה שלו עם שסתום לב טבעי, אשר בטווח הארוך די ריאלי בשל פיתוח הנדסת רקמות.
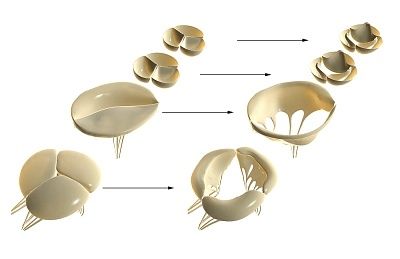
שסתומים הלב לפתח מן ניצנים עובריים של רקמת mesenchymal במהלך ההכנסה של endocardium. בתהליך של מורפוגנזה, התעלה האטריאנטריקולארית (שסתומי הלב וכלי הדם המיטרליים) ומערכת הלב בחדרית (אבי העורקים הלבביים).
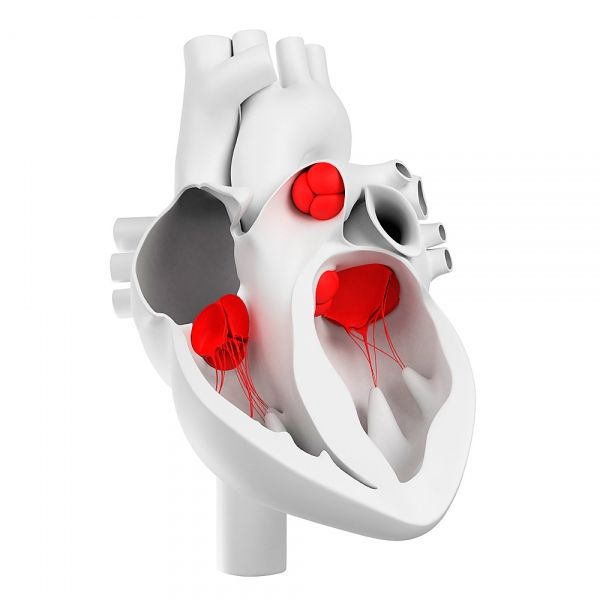
כיצד מסודרים שסתומי הלב?
תחילת המחקר של אספקת הדם לשסתומים הונחה על ידי Luschka (1852), תוך שימוש בהזרקה של כלי לב עם מסה מנוגדת. הוא מצא כלי דם רבים בשסתומים של השסתומים האטריוורנטולריים והסמינריים של אבי העורקים ועורק הריאה. עם זאת, בכמה מדריכים על האנטומיה הפתולוגית היסטולוגיה היו סימנים לכך מסתמי לב אנושיים ללא שינוי אינו מכילים כלי דם ו שייראה כאילו רק שסתום בתהליכים פתולוגיים שונים - טרשת של האטיולוגיה אנדוקרדיטיס השונות. מידע על היעדר כלי הדם התבסס בעיקר על מחקרים היסטולוגיים. ההנחה היתה כי בהיעדר כלי דם בחלק החופשי של השסתומים, התזונה שלהם מתרחשת על ידי סינון הנוזלים מפלסמה הדם המטאטאת את השסתומים. החדירה של כמה כלי עם סיבים של רקמת שריר מופשטים לתוך הבסיס של שסתומים ומיתרים גיד צוין.
עם זאת, כאשר כלי הזרקה של צבעים שונים בלב (פגר ב ג'לטין, מסקרה שחורה תרחיף מימית ג'לטין ביסמוט, פתרונות של ארגמן או כחול trypan), נמצא כי כלי לחדור שסתומים cerdechnye Atrio-חדרית, עורק אבי העורקים ריאתי יחד עם רקמת שריר הלב , מעט לא להגיע לקצה החופשי של העלה.
ברקמת החיבור הסיבית הנפרדת של שסתומי השסתומים האטריונטריקולריים, נמצאו כלים עיקריים נפרדים, עם anastomosing עם כלי מספר אזורים הממוקמים של רקמת שריר הלב.
המספר הגדול ביותר של כלי הדם היה ממוקם בבסיס פחות ופחות - בחלק החופשי של שסתומים אלה.
לדברי KI Kulchitsky et al. (1990), קוטר גדול יותר של כלי הדם והורידים נמצא בשסתום המיטרלי. בבסיס שסתומים של שסתום זה, יש בעיקר כלי הראשי עם רשת לולאה צרים של לולאה חודר לתוך החלק הבסיסי של השסתום ותופסת 10% משטחה. ב שסתום תלת מימדי, כלי הדם העורקים יש קוטר קטן יותר מאשר שסתום מיטרלי. בשסתומים של שסתום זה יש בעיקר כלי סוג מפוזרים לולאות רחב יחסית של נימי הדם. בשסתום המיטרלי, הדף הקדמי מזרם דם באופן אינטנסיבי יותר, בשסתום הטריוספידי, בשסתומים הקדמיים והאחוריים, הנושאים את פונקציית הסגירה העיקרית. היחס בין הקוטר של כלי הדם העורקים והוורידיים בשסתומים האטריונטריקולריים של לב האדם הבוגר הוא 1: 1.5. לולאות נימי הם מצולע ממוקם הניצב לבסיס של השסתומים דש. כלי שייט רשת מישורית הממוקם מתחת האנדותל מצד האנטריה. כלי הדם נמצאים גם במיתרי גיד, שם הם חודרים מן השרירים papillary של החדר הימני והשמאלי למרחק של עד 30% אורך של מיתרי גיד. כלי דם רבים יוצרים לולאות מקושתות בבסיס של מיתרי הגידים. שסתומי הלב של אבי העורקים וגזע ריאתי עבור אספקת הדם שונים באופן משמעותי מ atrioventricular. הכלים העיקריים של קוטר קטן יחסית מתאימים את הבסיס של שסתומי הסמינאר של שסתומי אבי העורקים וריאות. הענפים הקצרים של כלי אלה מסתיימים בלולאות נימיות של צורה סגלגל ו סגלגל לא סדיר. הם ממוקמים, בעיקר, ליד בסיס כנפי הסמיונר. כלי הדם הוורידים בבסיס של שסתומי אבי העורקים ועורק הריאה גם בקוטר קטן יותר מאשר בבסיס של שסתומים אטריובנטריקולריים. היחס בין הקוטר של כלי הדם העורקים והוורידיים בשסתומים של אבי העורקים והעורק הריאתי של לב האדם הבוגר הוא 1: 1.4. מן כלי גדול יותר, ענפים לרוחב קצר להסתעף, מסתיים נימים של הצורה האובלית ואת מצולע הלא נכון.

עם גיל ישן התחספסות סיבי רקמת החיבור כגון קולגן ואלסטין, כמו גם צמצום מספר רקמת חיבור סדיר רופפת סיבית מפתחת רקמות דשי טרשת שסתומים הפרוזדורי-חדרי ואת העלונים של שסתומי semilunar של אב העורקים ועורק הריאתי. סיבים באורך מופחתים שסתומי רקמת שריר מפוספסי לב ולכן מפחית וכמותו ומספר החודר לתוך הלב שסתומים כלי דם. בקשר עם השינויים הללו cerdechnye שסתום לאבד תכונות אלסטיות אלסטיות שלהם, אשר משפיעה על מנגנון הסגירה של השסתומים ופרמטרים המודינמיים.
שסתומי הלב יש רשתות נימי הלימפה ואת מספר קטן של כלי הלימפה מצויד בשסתומים. נימי הלימפה של השסתומים יש מראה אופייני: לומן שלהם הוא מאוד לא סדיר, נימי זהה באזורים שונים יש קוטר שונה. בצומת של כמה נימי דם, ההרחבות נוצרו-לקונות של צורות שונות. לולאות הרשת הן לעתים קרובות מצולע לא סדיר, לעתים קרובות צורה אליפסה או עגולה. לעתים קרובות, לולאות הרשת הלימפתיות אינן סגורות, והניימות הלימפטיות מסתיימות בעיוורון, לולאות נימי הלימפה מכוונות לעתים קרובות יותר מהקצה החופשי של השסתום לבסיס. בחלק מהמקרים נמצאה רשת דו-שכבתית של נימים לימפתיים בשסתומי השסתום האטריטרוטרי.
Plexuses העצבים של אנדוקרדיום ממוקמים בשכבות השונות שלה, בעיקר תחת האנדותל. בקצה החופשי של מדפי שסתומים, סיבי עצב ממוקמים, בעיקר רדיאלית, המתחברים לאלו של מיתרי הגידים. קרוב יותר לבסיס של השסתומים הוא מקלעת מקלעת גדולה המתחבר מקלעת סביב הטבעות סיבי. על השסתומים החצי, הרשת העצבית האנדוקרדיאלית נדירה יותר. במקום התקשרות של השסתומים, הוא הופך להיות עבה רב שכבתית.
מבנה נייד של שסתומי לב
שסתום התאים interstitial אחראי לשמירה על מבנה שסתום יש צורה מאורכת עם מספר רב של תהליכים רזים הנמשכים דרך כל המטריצה שסתום. ישנן שתי אוכלוסיות של תאים שסתומים interstitial, שונה במורפולוגיה ומבנה; כמה מהם יש תכונות התכווצות מאופיינים על ידי נוכחות של fibrils התכווצות, לאחרים יש תכונות הפרשה ויש להם reticulum endoplasmic מפותחים ומנגנון Golgi. הפונקציה התכווצות מתנגד ללחץ ההמודינמי והוא נתמך גם על ידי הפקה של חלבונים קרדיאליים וגם שלד, הכוללים את השרשראות הכבדות של אלפא ביתא מיוזין ו isoformform שונים של טרופונין. צמצום השסתום של שסתום הלב הודגם בתגובה למספר סוכנים vasoactive המציעים את הפעולה המתואמת של הגירוי הביולוגי לתפקוד מוצלח של השסתום.
תאים interstitial הם גם המרכיבים הדרושים של מערכת רדוקטיבית של מבנים כגון שסתומי הלב. התנועה המתמדת של השסתומים ואת העיוות של רקמת החיבור המשויכת אליו, מייצרת נזק אשר שסתום תאים interstitial להגיב כדי לשמור על שלמות השסתום. תהליך ההחלמה חיוני לתפקוד תקין של השסתום, והעדר תאים אלה במודלים מודרניים של שסתומים מלאכותיים הוא ככל הנראה גורם התורם לנזק המבני לביופרוסטזה.
כיוון חשוב בחקר תאי הביניים הוא לימוד האינטראקציה בינם לבין המטריצה שמסביב, בתיווך ההדבקה המוקדית של המולקולות. הדבקה מוקדית הם מיוחדים אינטראקציות תא מטריקס כי לקשור את השלד של תא לתאי חלבונים באמצעות integrins. הם משמשים גם כאתרי איתות להולכה, המשדרים מידע מכני מן המטריצה החוץ-תאית, אשר יכולים לעורר תגובות, כולל אך לא רק, הידבקות תאים, הגירה, צמיחה והבחנה. הבנת הביולוגיה הסלולרית של תאים intervitial valvular הוא חיוני להקמת המנגנונים שבאמצעותם תאים אלה אינטראקציה אחד עם השני ואת הסביבה, כך שניתן לשכפל את הפונקציה הזאת שסתומים מלאכותיים.
בקשר עם הפיתוח של אזור מבטיח של מחקר שסתום לב הנדסת רקמות interstitsiapnyh תאים נעשים תוך שימוש במגוון רחב של טכניקות. לאחר תוקף שלד התא של תאים מכתימים עבור vimentin, desmin, טרופונין, אלפא-תקטין שרירן חלקת שריר אלפא שרשרת כבדה וקלה בטא-מיוזין שרשרת-2 שרירן לב, אלפא-בטא טובולין. תאי התכווצות אשרו תשובה חיובית epinefrin, אנגיוטנסין II, ברדיקינין, carbachol, אשלגן כלורי, I. האנדותל יחסים פונקציונליים סלולר נקבעו ומאומת מחוררים אינטראקציות karboksiflyuorestseina microinjection. הפרשת מטריקס מותקן מכתים עבור prolyl-4-hydroxylase / סוג II קולגן, פיברונקטין, כונדרואיטין סולפט, laminin. עצבוב מותקן קצות עצבים מוטוריים קרובים קרבה, אשר משפיע על הפעילות של hydroxylase טירוזין ונוירופפטידים Y, אצטילכולין, פוליפפטיד מעי vasoactive, חומר P, kaptsitonin פפטיד הקשורים גן. גורמי Mitogenic העריכו בירושה גורמים טסיות-צמיחה, גורם גדילה פיברובלסטים בסיסית, סרוטונין (5-HT). פיברובלסטים למדו תאי ביניים מאופיינים קרום מרתף שלם, ארוך, תהליכים ציטופלסמית דקים חיבור קרוב המטריקס, reticulum endoplasmic המחוספס מפותח ואת המערכה גולג'י, העושר של microfilaments, היווצרות קשר דבק.
תאים endocardial Valvular טופס המעטפה atrombogenous תפקודית סביב כל שסתום הלב, בדומה האנדותל כלי הדם. השיטה הנפוצה של החלפת שסתום מבטלת את הפונקציה המגן של endocardium, אשר יכול להוביל לתצהיר של טסיות ופיברין על שסתומים מלאכותיים, התפתחות של זיהום חיידקי וסתיידות רקמות. עוד פונקציה אפשרית של תאים אלה הוא ויסות של תאים intervitial valvular הבסיסית, בדומה הרגולציה של תאי שריר חלק על ידי האנדותל. אינטראקציה מורכבת קיימת בין האנדותל לתאים הסמוכים, מתווכת חלקית על ידי גורמים מסיסים המופרשים על ידי תאי האנדותל. תאים אלה יוצרים משטח ענק, מכוסה בגידולים מיקרוניים בצד הלומינלי, ובכך מגדילים את החשיפה ואת האינטראקציה האפשרית עם החומרים המטבוליים של הדם המסתובב.
האנדותל קרובה מציגה הבדלים מורפולוגיים ופונקציונליים הנגרמים על ידי מאמצי גזירה על קיר הכלי המתרחשים במהלך התנועה של דם, ואותו חל על שסתום תאי endocardial קבלה הוא להאריך וצורה מצולעים. שינויים במבנה התא יכולים להתרחש בשל פעולת המודינמיקה המקומית על מרכיבי שלד התא של התא או את ההשפעה המשנית שנגרמת על ידי שינויים במטריצה תאיים הבסיסית. ברמה של תאים valvular valvular endocular יש חיבורים בין תאיים, שלפוחיות פלזמה, reticulum endoplasmic אחיד ואת המנגנון Golgi. למרות העובדה שהם מייצרים גורם פון Willebrand, הן in vivo ו בסביבה מלאכותית, הם חסרים את עגל Weibel-Palade (גרגרים ספציפיים המכילים גרם פון Willebrand), אשר הם אברונים ספציפיים האנדותל של כלי הדם. תאים endocardial valvular מאופיינים במפרקים חזקים, אינטראקציות פער פונקציונלי חופפים בקפלים שוליים.
תאים Endocardial לשמור על פעילות מטבולית שלהם אפילו במבחנה: ליצור Willebrand גורם, prostacyclin, פעילות התערוכה synthase תחמוצת חנקתית של האנזים המרת אנגיוטנסין, הדבקה מבודד מאוד מולקולות ICAM-1 ו עילם-1, כי הם קריטיים עבור עקדת תאים חד גרעיניים בפיתוח התגובה החיסונית. כל סמנים אלה צריכים להיכלל לטיפוח התרבות התא אידיאלי ליצירת שסתום מלאכותי על ידי הנדסת רקמות, אבל את הפוטנציאל immunostimulatory של תאים שסתום endocardial עצמם יכולים להגביל את השימוש בהם.
תאיים קומסקור לב שסתום מורכב קולגן סיבי האלסטין מקרומולקולות של proteoglycans ו גליקופרוטאינים. קולגן הוא - 60% מהמשקל היבש של השסתום, אלסטין - 10% ו proteoglycans - 20%. רכיב הקולגן מספק את היציבות המכנית הבסיסית של השסתום ומיוצג על ידי collagens I (74%). (24%) ו- V (2%). חבורות של חוטים קולגן מוקפים נדן אלסטין כי אינטראקציה ביניהם. שרשראות הצד גליקוז של מולקולות proteoglycan נוטים ליצור חומר דמוי ג'ל, שבו מולקולות אחרות אינטראקציה כדי ליצור חיבורים מטריקס קבע ורכיבים אחרים מופקדים. שסתום אדם לב glycosaminoglycans מורכב בעיקר של חומצה היאלורונית, ובמידה פחותה - של סולפט dermatan, כונדרואיטין-4-סולפט כונדרואיטין-6-סולפט, עם מינימום של סולפט heparan. שיפוץ ורקמות עדכון מטריקס מוסדרים על ידי metalloproteinases מטריצה (MMPs) ומעכבי הרקמות שלהם (TI). מולקולות אלה מעורבים גם במגוון רחב של תהליכים פיזיולוגיים ופתולוגיים חלק metalloproteinases, כולל collagenase ביניים (MMP-1, MMP-13) ו gelatinases (MMP-2, MMP-9) ומעכבי רקמות שלהם (TI-1, חמש 2, TI-3), נמצאים בכל שסתומי הלב. תוצרת היצע metalloproteinases מאפיין תנאים פתולוגיים של שסתום הלב.
 [6], [7], [8], [9], [10], [11], [12], [13], [14], [15], [16]
[6], [7], [8], [9], [10], [11], [12], [13], [14], [15], [16]
שסתומי הלב והמבנה המורפולוגי שלהם
שסתומי הלב מורכבים משלוש שכבות שונות מבחינה מורפולוגית ופונקציונלית של המטריצה של השסתום - סיבי, ספוגי וחדר חדר.
שכבת סיבי יוצר מסגרת הוכחה לטעון של שסתום דש, המורכב שכבות של סיבי קולגן. סיבים אלה מסודרים בצורה רדיאלית בצורה של קפלים עבור האפשרות של מתיחה שסתומים עורק עם סגירת. השכבה הסיבית שוכנת סמוך לשקע החיצוני של השסתומים. השכבות הסיביות של השסתומים האטריונטריקולריים משמשות המשך לקורות הקולגן של מיתרי הגידים. הוא ממוקם בין ספוגי (כניסה) ו חדרית (היציאה) שכבות.
בין הסיבי חדרית יש שכבת ספוגי (spongiosa). השכבה הספוגית מורכבת מרקמת חיבור מאורגנת היטב במדיום צמיג. המרכיבים המטריקס הדומיננטי של שכבה זו הם proteoglycans עם קולגן בכיוון שרירותי שכבות דקות של אלסטין. שרשראות הצד של המולקולות של proteoglycans לשאת מטען שלילי חזק, אשר משפיע על היכולת הגבוהה שלהם לאגד מים וליצור את הג'ל נקבובי של המטריצה. שכבת המטריצה הספוגית מפחיתה את הלחץ המכני בשסתומי שסתומי הלב ושומרת על גמישותם.
שכבת חדרית הוא הרבה יותר רזה מאחרים, והוא מלא סיבים אלסטיים המאפשרים רקמות לעמוד בפני עיוות קבוע. Elastin יש מבנה ספוגי המקיף ומחבר סיבי קולגן, ומבטיח תחזוקה שלהם במצב מקופל ניטרלי. שכבת הכניסה של השסתום (חדר הלב - עבור שסתומים עורקיים וספוגי - עבור אטריובנטריקולריים) מכיל יותר אלסטין מאשר הפלט, אשר מספק ריכוך של ההשפעה הידראולית בעת סגירת השסתומים. הקשר בין קולגן ואלסטין מאפשר הרחבה של השסתומים ל -40% ללא עיוות קבוע. תחת ההשפעה של עומס קטן, מבנים קולגן של שכבה זו מכוונים בכיוון של העמסה, ואת ההתנגדות שלה לצמיחה נוספת של העומס עולה.
לכן, הרעיון של שסתומי הלב ככפילות של אקולדיום לא פעיל הוא לא רק פשטני, אלא גם, למעשה, לא נכון. שסתומי הלב הם איבר בעל מבנה מורכב, כולל סיבי שריר מופשטים, דם וכלי הלימפה ואלמנטים עצביים. הן במבנה שלהם והן בתפקודם, השסתומים יוצרים שלם אחד עם כל מבני הלב. ניתוח התפקוד הרגיל של השסתום חייב לקחת בחשבון את הארגון הסלולרי שלו, כמו גם את האינטראקציה של התאים בינם לבין המטריצה. הידע שנצבר ממחקרים כאלה מוביל בעיצוב ופיתוח של החלפת שסתום באמצעות הנדסת רקמות.

