המומחה הרפואי של המאמר
פרסומים חדשים
טיפול בספסיס חמור ובהלם ספטי
סקירה אחרונה: 04.07.2025

כל תוכן iLive נבדק מבחינה רפואית או נבדק למעשה כדי להבטיח דיוק עובדתי רב ככל האפשר.
יש לנו קווים מנחים קפדניים המקור רק קישור לאתרים מדיה מכובד, מוסדות מחקר אקדמי, בכל עת אפשרי, עמיתים מבחינה רפואית מחקרים. שים לב שהמספרים בסוגריים ([1], [2] וכו ') הם קישורים הניתנים ללחיצה למחקרים אלה.
אם אתה סבור שתוכן כלשהו שלנו אינו מדויק, לא עדכני או מפוקפק אחרת, בחר אותו ולחץ על Ctrl + Enter.
טיפול יעיל בספסיס אפשרי רק באמצעות חיטוי כירורגי מלא של אזור הזיהום וטיפול אנטי-מיקרוביאלי הולם. טיפול אנטי-מיקרוביאלי ראשוני לא מספק מהווה גורם סיכון למוות בחולים עם ספסיס. שמירה על חיי המטופל, מניעה וסילוק של תפקודי איברים אפשריים רק באמצעות טיפול נמרץ ממוקד.
מטרתו העיקרית היא לייעל את הובלת החמצן (O2) בתנאים של צריכה מוגברת שלו, האופיינית לאלח דם חמור ולהלם ספטי. טיפול זה מיושם באמצעות תמיכה המודינמית ונשימתית.
תמיכה המודינמית
טיפול עירוי
טיפול עירוי הוא אחד האמצעים הראשוניים לשמירה על המודינמיקה, ומעל הכל, על תפוקת הלב. משימותיו העיקריות בחולים עם אלח דם הן:
- שחזור של זרימת דם מספקת לרקמות,
- תיקון הפרעות הומאוסטזיס,
- נורמליזציה של חילוף החומרים התאי,
- הפחתה בריכוז של מתווכים ספטיים ומטבוליטים רעילים.
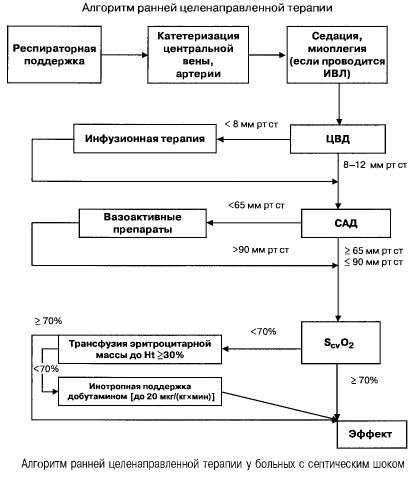
בספסיס עם אי ספיקת איברים מרובה והלם ספטי, הם מנסים להשיג במהירות (בתוך 6 השעות הראשונות) את הערכים הבאים של אינדיקטורים חשובים:
- המטוקריט >30%,
- דיאורזה 0.5 מ"ל/(ק"ג) לשעה,
- רוויון דם בווריד הנבוב העליון או בפרוזדור הימני >70%,
- לחץ דם ממוצע >65 מ"מ כספית,
- CVP 8-12 מ"מ כספית
שמירה על ערכים אלו ברמה שצוינה משפרת את שרידות המטופל (קטגוריית ראיות B). ניטור המודינמי באמצעות קטטר Swan-Ganz וטכנולוגיית PICCO (תרמודילוציה טרנספולמונית ואנליזת גלי דופק) מרחיבים את האפשרויות לניטור והערכת יעילות הטיפול ההמודינמי, אך אין ראיות לכך שהם משפרים את שרידות המטופל.
ערך העומס המקדים האופטימלי נבחר באופן אינדיבידואלי, מכיוון שיש צורך לקחת בחשבון את מידת הנזק לאדותל ואת מצב הניקוז הלימפטי בריאות, את התפקוד הדיאסטולי של החדרים ואת השינויים בלחץ התוך-בית-חזה. נפח טיפול העירוי נבחר כך ש-PCWP לא יעלה על COP בפלזמה (מניעת OL) ותהיה עלייה ב-CO. בנוסף, נלקחים בחשבון הפרמטרים המאפיינים את תפקוד חילוף הגזים של הריאות (paO2 ו- paO2 / FiO2 ) ושינויים בתמונה הרדיולוגית.
עבור טיפול עירוי כחלק מהטיפול הממוקד בספסיס ובהלם ספטי, משתמשים בתמיסות קריסטלואידיות וקולואידיות עם תוצאות כמעט זהות.
לכל מדיום העירוי יש יתרונות וחסרונות כאחד. כיום, בהתחשב בתוצאות מחקרים ניסויים וקליניים, אין סיבה להעדיף סוג מסוים.
- לדוגמה, לתיקון הולם של החזר הוורידי ורמת העומס המקדים, יש צורך לתת נפח של קריסטלואידים גדול פי 2-4 מזה של קולואידים, דבר הקשור למאפייני פיזור התמיסה בגוף. בנוסף, עירוי קריסטלואידים קשור לסיכון גבוה יותר לבצקת רקמות, והשפעתם ההמודינמית קצרה יותר מזו של קולואידים. יחד עם זאת, קריסטלואידים זולים יותר, אינם משפיעים על פוטנציאל הקרישה ואינם מעוררים תגובות אנפילקטואידיות. בהתבסס על האמור לעיל, ההרכב האיכותי של תוכנית העירוי נקבע בהתאם למאפייני המטופל, תוך התחשבות במידת ההיפוולמיה, שלב תסמונת DIC, נוכחות בצקת היקפית וריכוז האלבומין בסרום הדם, חומרת פגיעה ריאתית חריפה.
- תחליפי פלזמה (דקסטרנים, תכשירי ג'לטין, עמילן הידרוקסיאתיל) מסומנים במקרים של מחסור חמור ב-BCC. עמילני הידרוקסיאתיל בעלי דרגת החלפה של 200/0.5, 130/0.4 ו-130/0.42 הם בעלי יתרון פוטנציאלי על פני דקסטרנים עקב סיכון נמוך יותר לדליפת ממברנה והיעדר השפעה משמעותית קלינית על המוסטאזיס.
- הכנסת אלבומין במצבים קריטיים עלולה להגביר את הסיכון למוות. העלייה ב-COP במהלך עירויו היא חולפת, ולאחר מכן, בתנאים של חדירות מוגברת של מצע הנימים (תסמונת "דליפת הנימים"), מתרחשת אקסטרווזציה נוספת של אלבומין. ייתכן שעירוי אלבומין יהיה שימושי רק אם ריכוזו בסרום נמוך מ-20 גרם/ליטר ואין סימנים של "דליפה" לתוך האינטרסטיציום.
- השימוש בקריופלזמה מסומן עבור קרישת דם (קואגולופתיה כתוצאה מצריכה) וירידה בפוטנציאל הקרישה של הדם.
- יש להגביל את השימוש הנרחב במסת תאי דם אדומים מתורמים עקב הסיכון הגבוה לפתח סיבוכים שונים (APL, תגובות אנפילקטיות וכו'). לדברי רוב המומחים, ריכוז ההמוגלובין המינימלי בחולים עם אלח דם חמור הוא 90-100 גרם/ליטר.
תיקון של תת לחץ דם
לחץ פרפוזיה נמוך דורש הפעלה מיידית של תרופות המגבירות את טונוס כלי הדם ו/או את התפקוד האינוטרופי של הלב. דופמין או נוראפינפרין הן תרופות קו ראשון לתיקון לחץ דם נמוך בחולים עם הלם ספטי.
דופמין (dopmin) במינון של <10 מק"ג/(ק"ג x דקה) מעלה את לחץ הדם, בעיקר על ידי העלאת CO, ויש לו השפעה מינימלית על ההתנגדות הסיסטמית של כלי הדם. במינונים גבוהים, ההשפעה ה-α-אדרנרגית שלו דומיננטית, מה שמוביל להתכווצות כלי דם עורקית, ובמינון של <5 מק"ג/(ק"ג x דקה) דופמין מגרה קולטנים דופמינרגיים של כלי דם כלייתיים, מזנטריים וכליליים, מה שמוביל להרחבת כלי דם, סינון גלומרולרי מוגבר והפרשת Na+.
נוראפינפרין מעלה את לחץ הדם העורקי הממוצע ומגביר את הסינון הגלומרולרי. אופטימיזציה של ההמודינמיקה הסיסטמית תחת פעולתו מובילה לשיפור תפקוד הכליות ללא שימוש במינונים נמוכים של דופמין. מחקרים בשנים האחרונות הראו כי שימוש בודד, בהשוואה לשילוב עם מינונים גבוהים של דופמין, מוביל לירידה משמעותית סטטיסטית בתמותה.
אדרנלין הוא תרופה אדרנרגית בעלת תופעות הלוואי ההמודינמיות הבולטות ביותר. יש לו השפעה תלוית מינון על קצב הלב, לחץ הדם העורקי הממוצע, תפוקת הלב, תפקוד החדר השמאלי, ואספקה וצריכת חמצן . עם זאת, טכיאריתמיות, הידרדרות בזרימת הדם באיברים והיפרלקטטמיה מתרחשות בו זמנית. לכן, השימוש באדרנלין מוגבל למקרים של עמידות מוחלטת לקטכולאמינים אחרים.
דובוטמין היא התרופה המועדפת להגברת אספקת וצריכת CO ו-O2 בעומס מוקדם תקין או מוגבר. בשל פעולתו העיקרית על קולטני בטא 1-אדרנרגיים, היא יעילה יותר מדופמין בהגברת פרמטרים אלה.
מחקרים ניסויים הראו כי קטכולאמינים, בנוסף לתמיכה במחזור הדם, יכולים לווסת את מהלך הדלקת הסיסטמית על ידי השפעה על הסינתזה של מתווכים מרכזיים עם השפעה מרוחקת. תחת השפעת אדרנלין, דופמין, נוראדרנלין ודובוטמין, מקרופאגים מופעלים מפחיתים את הסינתזה וההפרשה של TNF-α.
בחירת חומרים אדרנרגיים מתבצעת לפי האלגוריתם הבא:
- מדד לב 3.5-4 ליטר/(דקה x מ"ר ), SvO2 > 70% - דופמין או נוראפינפרין,
- מדד לב <3.5 l/(דקה x מ"ר ), SvO2 < 70% - דובוטמין (אם לחץ דם סיסטולי <70 מ"מ כספית - יחד עם נוראפינפרין או דופמין).
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ]
תמיכה נשימתית
הריאות הן בין איברי המטרה הראשונים המעורבים בתהליך הפתולוגי בספסיס. אי ספיקת נשימה חריפה היא אחד המרכיבים המובילים בתפקוד לקוי של איברים מרובים. הביטויים הקליניים והמעבדתיים שלה בספסיס תואמים ל-ALI, ועם התקדמות התהליך הפתולוגי - ARDS. האינדיקציות לאוורור מכני בספסיס חמור נקבעות בהתאם לחומרת אי ספיקת הנשימה הפרנכימטית (ARF או ARDS). הקריטריון שלה הוא מדד הנשימה:
- <200 - אינטובציה של קנה הנשימה ותמיכה נשימתית מסומנים,
- >200 - הקריאות נקבעות באופן פרטני.
אם המטופל בהכרה במהלך נשימה ספונטנית עם תמיכה בחמצן, אין הוצאה גבוהה על עבודת הנשימה וטכיקרדיה בולטת (דופק דופק <120 לדקה), הערך הנורמלי של החזרה הוורידית SO2 > 90%, אז ניתן להימנע מהעברתו לאוורור מלאכותי. עם זאת, יש צורך לעקוב בקפידה אחר מצבו של המטופל. הערך האופטימלי של SO2 הוא כ-90%. ניתן לשמור עליו באמצעות שיטות שונות של אספקת גז (מסכות פנים, צנתרים לאף) בריכוזים לא רעילים (FiO2 < 0.6). אוורור מלאכותי לא פולשני אינו מומלץ באלח דם (קטגוריית ראיות B).
יש להימנע ממצבי אוורור מכני בנפח גבוה (MVV) (VO = 12 מ"ל/ק"ג), שכן במקרים כאלה הפרשת ציטוקינים מהריאות גוברת, מה שמוביל להחמרה של MOF. יש צורך לדבוק ברעיון של אוורור מכני בטוח, דבר האפשרי אם מתקיימים התנאים הבאים (קטגוריית ראיות A):
- DO <10 מ"ל/ק"ג,
- יחס שאיפה ונשיפה לא הפוך,
- לחץ אוויר מקסימלי <35 ס"מ H2O,
- FiO2 <0.6 .
בחירת פרמטרי מחזור הנשימה מתבצעת עד להשגת אוורור מכני מספק, הקריטריונים שלה הם paO2 > 60 מ"מ כספית, SpO2 > 88-93%, pvO2 35-45 מ"מ כספית, SvO2 > 55%.
אחת השיטות היעילות לייעול חילוף הגזים היא ביצוע הנשמה מלאכותית בתנוחת שכיבה (Prone Positioning) (קטגוריית ראיות B). תנוחה זו יעילה בחולים במצב החמור ביותר, אם כי השפעתה על הפחתת התמותה בטווח הארוך אינה מובהקת סטטיסטית.
תמיכה תזונתית
ביצוע תמיכה תזונתית מלאכותית הוא מרכיב חשוב בטיפול, אחד האמצעים המחייבים, שכן התפתחות תסמונת אי ספיקת איברים מרובה בספסיס מלווה בדרך כלל בביטויים של היפרמטבוליזם. במצב כזה, צורכי האנרגיה מסופקים על ידי הרס מבנים תאיים של האדם עצמו (אוטוקניבליזם), מה שמחמיר את תפקוד האיברים ומגביר את האנדוטוקסיקוזיס.
תמיכה תזונתית נחשבת כשיטה למניעת תשישות חמורה (מחסור בחלבון-אנרגיה) על רקע עלייה ניכרת בקטליזציה ובמטבוליזם. הכללת תזונה אנטרלית במכלול הטיפול האינטנסיבי מונע את תנועת המיקרופלורה במעי, דיסבקטריוזיס, מגביר את הפעילות התפקודית של אנטרוציטים ואת התכונות המגנות של רירית המעי. גורמים אלה מפחיתים את מידת האנדוטוקסיקוזיס ואת הסיכון לסיבוכים זיהומיים משניים.
חישוב תמיכה תזונתית:
- ערך אנרגטי - 25-35 קלוריות/(ק"ג משקל גוף x יום),
- כמות חלבון - 1.3-2.0 גרם/(ק"ג משקל גוף x יום),
- כמות פחמימות (גלוקוז) - פחות מ-6 גרם/ק"ג/יום,
- כמות שומן - 0.5-1 גרם/ק"ג/יום,
- דיפפטידים של גלוטמין 0.3-0.4 גרם/ק"ג/יום,
- ויטמינים - מנה יומית סטנדרטית + ויטמין K (10 מ"ג/יום) + ויטמינים B1 ו- B6 ( 100 מ"ג/יום) + ויטמינים A, C, E
- מיקרו-אלמנטים - מנה יומית סטנדרטית + אבץ (15-20 מ"ג/יום + 10 מ"ג/יום בנוכחות צואה רכה),
- אלקטרוליטים - Na+, K+, Ca2+ לפי חישובי איזון וריכוז בפלזמה.
התחלה מוקדמת של תמיכה תזונתית (24-36 שעות) יעילה יותר מאשר ביום השלישי-רביעי של טיפול אינטנסיבי (קטגוריית ראיות B), במיוחד עם הזנה דרך צינור אנטרלי.
באלח דם חמור, אין יתרונות להזנה אנטרלית או פרנטרלית; משך תפקוד לקוי של האיברים ומשך התמיכה הנשימתית והאינוטרופית זהים, ושיעורי התמותה זהים. בהתחשב באמור לעיל, הזנה אנטרלית מוקדמת היא אלטרנטיבה זולה יותר להזנה פרנטרלית. השימוש בתערובות מועשרות בסיבים תזונתיים (פרה-ביוטיקה) להזנה דרך צינור מפחית משמעותית את שכיחות השלשולים בחולים עם אלח דם חמור.
לסינתזת חלבונים יעילה בגוף, חשוב לשמור על יחס מטבולי של "חנקן כולל, גרם - קלוריות שאינן חלבוניות, קק"ל" = 1-(110-130). המינון המקסימלי של פחמימות הוא 6 גרם / (ק"ג משקל גוף ליום), מכיוון שהכנסת מינונים גדולים מאיימת על היפרגליקמיה והפעלת קטבוליזם בשרירי השלד. מומלץ לתת אמולסיות שומן מסביב לשעון.
התוויות נגד לתמיכה תזונתית:
- חמצת מטבולית לא מפוצה,
- אי סבילות אישית למדיה תומכת תזונתית,
- היפוולמיה חמורה שלא החלימה,
- הלם עמיד - מינון דופמין >15 מק"ג/(ק"ג x דקות) ולחץ דם סיסטולי <90 מ"מ כספית,
- היפוקסמיה עורקית קשה ובלתי מטופלת.
שליטה גליקמית
היבט חשוב בטיפול מורכב בספסיס חמור הוא ניטור מתמיד של ריכוז הגלוקוז בפלזמת הדם וטיפול באינסולין. גליקמיה גבוהה והצורך בתיקונה הם גורמים לתוצאה שלילית בספסיס. בהתחשב בנסיבות הנ"ל, רמות גליקמיה נורמליות (4.5-6.1 mmol/l) נשמרת אצל חולים, וכאשר ריכוז הגלוקוז עולה מעל הערכים המקובלים, מתבצע עירוי אינסולין (0.5-1 U/h). בהתאם למצב הקליני, ריכוז הגלוקוז מנוטר כל 1-4 שעות. בעת יישום אלגוריתם זה, נצפתה עלייה מובהקת סטטיסטית בהישרדות החולים.
 [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ]
[ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ]
גלוקוקורטיקואידים
תוצאות המחקרים המודרניים בנוגע ליעילות השימוש בגלוקוקורטיקואידים בחולים עם הלם ספטי מסוכמות בהצהרות הבאות:
- לא מתאים להשתמש בהורמונים במינונים גבוהים [מתילפרדניזולון 30-120 מ"ג/(ק"ג x יום) פעם אחת או למשך 9 ימים, דקסמתזון 2 מ"ג/(ק"ג x יום) למשך יומיים, בטאמתזון 1 מ"ג/(ק"ג x יום) למשך 3 ימים] - סיכון מוגבר לזיהומים בבית חולים, אין השפעה על ההישרדות,
- השימוש בהידרוקורטיזון במינון של 240-300 מ"ג ליום למשך 5-7 ימים מאיץ את ייצוב הפרמטרים ההמודינמיים, מאפשר הפסקת תמיכה וסקולרית ומשפר את ההישרדות בחולים עם אי ספיקה יחסית של בלוטת יותרת הכליה (קטגוריית ראיות B).
יש צורך לנטוש את המרשם האמפירי הכאוטי של פרדניזולון ודקסמתזון - אין עילה להסקת מידע חדש עליהם. בהיעדר ראיות מעבדתיות לאי ספיקת יותרת הכליה יחסית, מנוהל הידרוקורטיזון במינון של 300 מ"ג ליום (ב-3-6 זריקות).
- בהלם עמיד,
- אם נדרשים מינונים גבוהים של ווזופרסורים כדי לשמור על המודינמיקה יעילה.
ייתכן שבמצבים של דלקת סיסטמית בהלם ספטי, יעילות ההידרוקורטיזון קשורה להפעלת מעכב הגורם הגרעיני kB (NF-kB-a) ולתיקון אי ספיקה יחסית של בלוטת יותרת הכליה. בתורו, עיכוב פעילות הגורם הגרעיני שעתוק (NF-kB) מוביל לירידה ביצירת סינתטאז NO מושרה (NO הוא מרחיב כלי הדם האנדוגני החזק ביותר), ציטוקינים מעודדי דלקת, COX ומולקולות הידבקות.
חלבון C מופעל
אחת התופעות האופייניות לאלח דם היא הפרעה בקרישה מערכתית (הפעלת מפל הקרישה ועיכוב פיברינוליזה), מה שמוביל בסופו של דבר להיפופרופוזיה ולתפקוד לקוי של איברים. השפעת חלבון C מופעל על המערכת הדלקתית מתממשת בכמה דרכים:
- הפחתת היצמדות סלקטין ללויקוציטים, אשר מגן על האנדותל מפני נזק, אשר ממלא תפקיד מפתח בהתפתחות דלקת מערכתית,
- ירידה בשחרור ציטוקינים ממונוציטים,
- חסימת שחרור TNF-α מלקוציטים לויקוציטים,
- עיכוב ייצור תרומבין (מגביר את התגובה הדלקתית).
פעולה נוגדת קרישה, פרופיברינוליטית ואנטי דלקתית
- חלבון C מופעל נובע מ
- פירוק גורמי Va ו-VIIIa - דיכוי היווצרות פקקים,
- דיכוי של מעכב פלסמינוגן - הפעלת פיברינוליזה,
- השפעה אנטי דלקתית ישירה על תאי אנדותל ונויטרופילים,
- הגנה על האנדותל מפני אפופטוזיס
מתן חלבון C פעיל [דרוטרקוגין אלפא (פעיל)] במינון של 24 מק"ג/(ק"ג שעה) למשך 96 שעות מפחית את הסיכון למוות ב-19.4%. אינדיקציות למתן: אלח דם עם MOF חריף וסיכון גבוה למוות (APACHE II > 25 נקודות, תפקוד לקוי של 2 איברים או יותר, קטגוריית ראיות B).
חלבון C פעיל אינו מפחית תמותה בילדים, חולים עם תפקוד לקוי של איבר בודד, APACHE II < 25 נקודות, בחולים עם אלח דם לא ניתוחי.
 [ 14 ], [ 15 ], [ 16 ], [ 17 ]
[ 14 ], [ 15 ], [ 16 ], [ 17 ]
אימונוגלובולינים
מומלץ מתן תוך ורידי של אימונוגלובולינים (IgG ו-IgG+IgM) קשור ליכולתם להגביל את הפעולה המוגזמת של ציטוקינים מעודדי דלקת, להגביר את סילוק האנדוטוקסינים וסופראנטיגן סטפילוקוקלי, לחסל אנרגיה ולשפר את ההשפעה של אנטיביוטיקה מסוג β-lactam. השימוש בהם בטיפול בספסיס חמור ובהלם ספטי הוא השיטה היחידה לתיקון חיסוני שמגדילה את ההישרדות. ההשפעה הטובה ביותר נרשמה בעת שימוש בשילוב של IgG ו-IgM [RR=0.48 (0.35-0.75), קטגוריית ראיות A]. משטר המינון הסטנדרטי הוא 3-5 מ"ל/(ק"ג x יום) במשך 3 ימים ברציפות. בעת שימוש באימונוגלובולינים, התוצאות האופטימליות ביותר הושגו בשלב המוקדם של ההלם ("הלם חם") ובחולים עם ספסיס חמור (ציון APACHE II של 20-25 נקודות).
מניעת טרומבוז ורידים עמוק
מניעת DVT בגפיים התחתונות משפיעה באופן משמעותי על תוצאות הטיפול בחולים עם אלח דם (קטגוריית ראיות A). למטרה זו משתמשים הן בהפרינים לא מופרדים והן בהפרינים בעלי משקל מולקולרי נמוך. היתרונות העיקריים של הפרינים בעלי משקל מולקולרי נמוך הם שכיחות נמוכה יותר של סיבוכים דימומיים, השפעה חלשה יותר על תפקוד טסיות הדם והשפעה ארוכת טווח (ניתן לתת אותם פעם ביום).
מניעת היווצרות כיבי לחץ במערכת העיכול
כיוון זה ממלא תפקיד משמעותי בתוצאה חיובית בטיפול בחולים עם אלח דם חמור והלם ספטי, שכן שיעור התמותה מדימום מפצעי לחץ במערכת העיכול הוא 64-87%. ללא אמצעי מניעה, פצעי לחץ מופיעים ב-52.8% מהחולים במצב קריטי. עם זאת, השימוש במעכבי משאבת פרוטון וחוסמי קולטן היסטמין H2 מפחית את הסיכון ביותר מפי 2 (קבוצת התרופות הראשונה יעילה יותר מהשנייה). כיוון המניעה והטיפול העיקרי הוא שמירה על רמת חומציות (pH) בטווח של 3.5-6.0. יש להדגיש כי בנוסף לתרופות הנ"ל, תזונה אנטרלית ממלאת תפקיד חשוב במניעת היווצרות פצעי לחץ.
טיהור דם חוץ גופי
חומרים ביולוגיים פעילים שונים ותוצרים מטבוליים המעורבים בהתפתחות דלקת כללית הם מטרות לשיטות ניקוי רעלים, דבר שחשוב במיוחד בהיעדר פינוי טבעי מהכבד במצבים של אי ספיקת איברים מרובה. שיטות טיפול חלופי בכליות נחשבות למבטיחות, מכיוון שהן יכולות להשפיע לא רק על הפרעות אורמיות בחולים עם אי ספיקת כליות, אלא גם להשפיע לטובה על שינויים אחרים בהומאוסטזיס ובתפקוד לקוי של איברים המתרחשים בספסיס, הלם ואי ספיקת איברים מרובה.
עד כה, אין נתונים המאשרים את הצורך להשתמש בשיטות טיהור דם חוץ-גופיות כאחד מכיווני הטיפול הפתוגנטי העיקריים בספסיס ובהלם ספטי. השימוש בהם מוצדק במקרה של אי ספיקת איברים מרובה עם דומיננטיות כלייתית.
 [ 18 ], [ 19 ], [ 20 ], [ 21 ], [ 22 ], [ 23 ]
[ 18 ], [ 19 ], [ 20 ], [ 21 ], [ 22 ], [ 23 ]
המודיאליזה
מהות השיטה היא דיפוזיה של חומרים בעלי משקל מולקולרי נמוך (עד 5x10³ דא ) דרך קרום חדיר למחצה וסילוק נוזלים עודפים מהגוף לאורך מפל לחץ. המודיאליזה נמצאת בשימוש נרחב לטיפול בחולים עם אי ספיקת כליות כרונית וחריפה כאחד. קצב דיפוזיה של חומרים תלוי באופן אקספוננציאלי במשקל המולקולרי שלהם. לדוגמה, סילוק האוליגופפטידים איטי יותר מהסינתזה שלהם.
המופילטרציה
המופילטרציה היא שיטה יעילה להסרת חומרים בעלי משקל מולקולרי של 5x10³ - 5x10³ דאל והדרך היחידה להסיר קבוצה גדולה של חומרים פעילים ביולוגית ומטבוליטים מהגוף. השיטה מבוססת על שיטת ההסעה של העברת מסה. בנוסף לתיקון הולם של אזוטמיה, המופילטרציה מסירה ביעילות אנפילטוקסינים C3a, C5a, ציטוקינים מעודדי דלקת (TNF-α, IL-1b, 6 ו-8), β2-מיקרוגלובולין, מיוגלובין, הורמון פאראתירואיד, ליזוזים (משקל מולקולרי - 6000 דאל), α-עמילאז (משקל מולקולרי - 36,000-51,000 דאל), קריאטין פוספקינאז, פוספטאז אלקליין, טרנסאמינאזות וחומרים אחרים. המופילטרציה מסירה חומצות אמינו וחלבוני פלזמה (כולל אימונוגלובולינים וקומפלקסים חיסוניים במחזור הדם).
המודיאפילטרציה
המודיאפילטרציה היא השיטה החזקה ביותר לטיהור דם, המשלבת דיפוזיה והסעה (כלומר, GD ו-GF). תרומה נוספת לתהליך ניקוי הרעלים נובעת מספיחת חומרים פתולוגיים על קרום המסנן.
פלסמפרזיס
פלסמפרזיס (חילוף פלזמה, סינון פלזמה) נחשבת גם כשיטה אפשרית לתיקון דלקת כללית בחולים עם אלח דם והלם ספטי. השיטה האופטימלית נחשבת לשימוש בחילוף פלזמה במצב רציף עם הוצאת 3-5 נפחים של פלזמה והחלפתה בו זמנית בתמיסות טריות קפואות, אלבומין, קולואידליות וקריסטלואידיות. עם מקדם סינון של 1, סינון פלזמה מבטיח הסרה טובה של חלבון C-ריאקטיבי, הפטוגלובין, מקטע משלים C3, 1-אנטיטריפסין, IL-6, טרומבוקסאן-B2, גורם מגרה גרנולוציטים, TNF. השימוש בסורבים לטיהור פלזמת המטופל מפחית את הסיכון לזיהום ומפחית את עלות ההליך, מכיוון שאין צורך להשתמש בחלבונים זרים.
שימוש בעירוי ממושך של נתרן סלניט (סלנאז) במינון של 1000 מק"ג/יום בספסיס חמור מוביל לירידה בתמותה.
סלניום הוא מיקרו-יסוד חיוני, שחשיבותו קשורה לתפקידו המרכזי במערכות נוגדות החמצון של התאים. רמת הסלניום בדם נשמרת בטווח של 1.9-3.17 מיקרומולר/ליטר. הצורך בסלניום הוא 50-200 מיקרוגרם ליום, והוא תלוי בזמינות של נוגדי חמצון ומיקרו-יסודות אחרים.
סלניום הוא נוגד חמצון רב עוצמה, מרכיב של גלוטתיון פראוקסידאז, פוספולין גלוטתיון פראוקסידאז, אוקסידורדוקטאזות אחרות וכמה טרנספראזות. גלוטתיון פראוקסידאז הוא החוליה החשובה ביותר במערכת נוגדת החמצון האנדוגנית.
יעילותו של סלניום במצבים קריטיים נחקרה בשנים האחרונות. מחקרים אלה הראו כי מנגנוני הפעולה העיקריים של סלניום הם:
- דיכוי היפר-אקטיבציה של NF-kB;
- ירידה באקטיבציה של משלים;
- פעולתו כאימונומודולטור, נוגד חמצון וסוכן אנטי דלקתי
- שמירה על ניצול מי חמצן;
- דיכוי הידבקות אנדותל (ביטוי מופחת של ICAM-1, VCAM-2,
- E - סלקטין, P - סלקטין);
- הגנה על האנדותל מפני רדיקלים אוקסיים (באמצעות סלנופרוטאין P, המונע היווצרות של פראוקסיניטריט מ-O2 ו- NO).
לסיכום האמור לעיל, נוכל להגדיר משימות ספציפיות של טיפול נמרץ עבור אלח דם חמור:
- תמיכה המודינמית: לחץ דם ורידי (CVP) 8-12 מ"מ כספית, לחץ דם ממוצע >65 מ"מ כספית, דיאורזה 0.5 מ"ל/(ק"ג שעה), המטוקריט >30%, רוויון דם ורידי מעורב >70%.
- לחץ אוויר שיא בתמיכה נשימתית <35 ס"מ H2O, מקטע חמצן שאיף <60%, נפח גאות <10 מ"ל/ק"ג, יחס שאיפה לנשיפה לא הפוך.
- גלוקוקורטיקואידים - "מינונים נמוכים" (הידרוקורטיזון 240-300 מ"ג ליום).
- חלבון C פעיל 24 מק"ג/(ק"ג שעה) למשך 4 ימים באלח דם חמור (APACHE II >25).
- טיפול חלופי אימונוקורקטיבי עם פנטגלובין.
- מניעת טרומבוז ורידים עמוק של הגפיים התחתונות.
- מניעת היווצרות כיבי לחץ במערכת העיכול: שימוש במעכבי משאבת פרוטונים וחוסמי קולטני H2-היסטמין.
- טיפול חלופי לאי ספיקת כליות חריפה.
- תמיכה תזונתית: ערך אנרגטי של מזון 25-30 קק"ל/ק"ג משקל גוף x יום), חלבון 1.3-2.0 גרם/(ק"ג משקל גוף x יום), גלוטמין דיפפטידים 0.3-0.4 גרם/(ק"ג x יום), גלוקוז - 30-70% מהקלוריות שאינן חלבון, בתנאי שרמת הגליקמיה נשמרת <6.1 מילימול/ליטר, שומנים - 15-50% מהקלוריות שאינן חלבון.

