המומחה הרפואי של המאמר
פרסומים חדשים
מום עורקי-ורידי
סקירה אחרונה: 04.07.2025

כל תוכן iLive נבדק מבחינה רפואית או נבדק למעשה כדי להבטיח דיוק עובדתי רב ככל האפשר.
יש לנו קווים מנחים קפדניים המקור רק קישור לאתרים מדיה מכובד, מוסדות מחקר אקדמי, בכל עת אפשרי, עמיתים מבחינה רפואית מחקרים. שים לב שהמספרים בסוגריים ([1], [2] וכו ') הם קישורים הניתנים ללחיצה למחקרים אלה.
אם אתה סבור שתוכן כלשהו שלנו אינו מדויק, לא עדכני או מפוקפק אחרת, בחר אותו ולחץ על Ctrl + Enter.
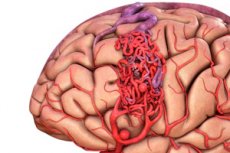
מום עורקי-ורידי הוא פגם מולד בהתפתחות כלי הדם, המאופיין בנוכחות רשת לא תקינה של אנסטומוזות עורקיות-ורידיות. לרוב, מומים עורקי-ורידיים ממוקמים בגומה האחורית של הגולגולת ובעלי מבנה טיפוסי למדי - עורק אמיתי אחד או שניים, סבך של ורידים עורקיים-ורידיים ווריד ניקוז אחד.
 [ 1 ]
[ 1 ]
גורם ל מום עורקי-ורידי
הגורמים שעשויים להיות בבסיס התפתחות AVM אינם מובנים במלואם, אך ההערכה היא שהם עשויים להיות קשורים לגורמים גנטיים וסביבתיים. להלן כמה מהגורמים האפשריים שעשויים להיות קשורים להתפתחות AVM:
- גורמים גנטיים: מחקרים הראו כי לחלק מהחולים עם AVMs יש היסטוריה משפחתית של המצב. מוטציות גנטיות עשויות למלא תפקיד בהיווצרות הפרעה בכלי הדם.
- פגמים מולדים: אנומליות מולדות בכלי הדם יכולות להתפתח במהלך ההתפתחות העוברית. אלה עשויות לנבוע משגיאות בהתפתחות רקמות כלי הדם של המוח.
- גורמים סביבתיים: מספר מחקרים הראו קשר בין מחלות רקע (AVM) לבין גורמים סביבתיים מסוימים, כגון חשיפה לקרינה או רעלים במהלך ההריון. עם זאת, קשרים אלה אינם תמיד מאושרים ואינם מסבירים את כל מקרי ה-AVM.
- גורמים אזוריים: במקרים מסוימים, AVM עשוי להיות קשור לאזורים גיאוגרפיים או לקבוצות אתניות מסוימות, אך קשרים אלה דורשים מחקר נוסף.
בנוסף לגורמים אלו שעשויים להשפיע על התפתחות AVM, חשוב לציין שמדובר במצב מולד ובדרך כלל מתגלה בלידה או בילדות המוקדמת, אם כי תסמינים עשויים להופיע מאוחר יותר בחיים. נדרש מחקר נוסף כדי להבין במדויק את הגורמים והמנגנונים להתפתחות AVM.
פתוגנזה
המסוכן ביותר הוא קרע בדפנות המום, המלווה בדימום תוך גולגולתי ספונטני. זה קורה עקב העובדה שדם מעורב זורם בכלי הדם המומים תחת לחץ קרוב לעורקים. ובאופן טבעי, לחץ גבוה מוביל למתיחה של כלי הדם שעברו שינוי ניווני, עלייה בנפחם ודילול הדופן. בסופו של דבר, קרע מתרחש במקום הדק ביותר. על פי נתונים סטטיסטיים, זה קורה ב-42-60% מהחולים עם AVM. התמותה בקרע AVM הראשון מגיעה ל-12-15%. בשאר, הדימום יכול לחזור על עצמו, ללא כל מחזוריות. צפינו בחולה שסבל מאחד עשר דימומים תוך גולגולתיים ספונטניים במשך 8 שנים. מהלך "שפיר" יחסית זה של קרע AVM בהשוואה לקרע של מפרצות עורקיות מוסבר על ידי המוזרויות של הפרעות המודינמיות המתרחשות לאחר הקרע. ידוע כי קרע של מפרצת עורקית מוביל לרוב לדימום תת-עכבישי (SAH) ולהתפתחות של אנגיוספזם, אשר בדקות הראשונות הוא בעל אופי מגן, מסייע לעצור במהירות את הדימום, אך לאחר מכן מהווה סכנה משמעותית לחייו של המטופל.
אנגיוספזם, המוביל לאיסכמיה מוחית ובצקת, הוא שקובע את חומרת מצבו של המטופל ואת הפרוגנוזה. לעומת זאת, אנגיוספזם של העורקים המביאים של ה-AVM, לעומת זאת, משפר את אספקת הדם למוח עקב ירידה בהפרשה עורקית-ורידית. כאשר ה-AVM נקרע, נוצרות לעתים קרובות יותר המטומות תוך-מוחיות ותת-דורליות. פריצת הדם לתוך ציסטרנות הסאבארכנואידיות היא משנית. הדימום מדופן הקרע של ה-AVM נעצר מהר יותר, מכיוון שלחץ הדם בו נמוך יותר מאשר בעורקים הראשיים והדופן רגישה יותר לדחיסה על ידי הדם שנשפך. באופן טבעי, זה לא תמיד נגמר טוב עבור המטופל. קרעי ה-AVM המסוכנים ביותר נמצאים ליד חדרי המוח, בגרעינים התת-קורטיקליים ובגזע המוח. אנגיוספזם של העורקים המביאים במצב זה מסייע לעצור את הדימום.
הגורם הקובע בפתוגנזה של קרע ב-AVM הוא נפח הדם שנשפך ולוקליזציה של ההמטומה. המטומות תוך-מוחיות חצי כדוריות, אפילו בנפח של עד 60 סמ"ק , מתקדמות בצורה חיובית יחסית. הן יכולות לגרום להפרעות נוירולוגיות מוקדיות קשות, אך לעיתים רחוקות מובילות להפרעות חיוניות קשות. קרע בהמטומה בחדרי המוח מחמיר משמעותית את הפרוגנוזה. מצד אחד, דם, המגרה את האפנדימה של החדרים, מגביר את ייצור הנוזל השדרתי, ומצד שני, המשפיע על תחתית החדר, מוביל להפרעות קשות בתפקודי המרכזים החיוניים הממוקמים בהיפותלמוס. התפשטות הדם בכל מערכת החדרים מובילה לטמפונדה של האחרונה, אשר כשלעצמה אינה תואמת את החיים.
דם שחדר לתוך ציסטרנות התת-עכבישיות משבש גם את זרימת הנוזל השדרתי, מה שמקשה על הנוזל השדרתי להגיע לגרגורי הפקיון החסומים בדם. כתוצאה מכך, ספיגת הנוזל השדרתי מואטת ועלול להתפתח יתר לחץ דם חריף של הנוזל השדרתי, ואחריו הידרוצפלוס פנימי וחיצוני. כתוצאה מפירוק היסודות שנוצרו מהדם שנשפך, נוצרים מספר רב של חומרים רעילים, שרובם בעלי השפעה כלי דם. מצד אחד, הדבר מוביל להתכווצות כלי דם של עורקי פיאל קטנים, ומצד שני, הוא מגביר את חדירות הנימים. תוצרי פירוק הדם משפיעים גם על תאי עצב, משנים את התהליכים הביוכימיים שלהם ומשבשים את חדירות קרומי התא. ראשית, תפקוד משאבת האשלגן-נתרן משתנה ואשלגן מתחיל לעזוב את התא, וקטיון הנתרן, שהוא הידרופילי פי ארבעה יותר מאשלגן, ממהר לתפוס את מקומו.
זה מוביל תחילה לבצקת תוך תאית באזור סביב הדימום, ולאחר מכן לנפיחות של התאים. היפוקסיה תורמת גם להתפתחות בצקת, אשר מצטרפת באופן בלתי נמנע עקב דחיסה של כלי המוח על ידי ההמטומה ועלייה בלחץ נוזל השדרה, כפי שכבר נאמר. תפקוד לקוי של החלקים הדיאנצפליים של המוח, ומעל הכל, ויסות מאזן המים-אלקטרוליטים, מוביל לאגירת נוזלים בגוף, אובדן אשלגן, מה שמגביר גם את התגובה הבצקתית של המוח. הפתוגנזה של קרע ב-AVM אינה מוגבלת להפרעות מוחיות. לא פחות מסוכנות סיבוכים חוץ-מוחיים. קודם כל, מדובר בתסמונת מוחית, אשר על האלקטרוקרדיוגרמה יכולה לדמות אי ספיקה כלילית חריפה.
די מהר, חולים עם דימומים תוך-מוחיים מפתחים דלקת ריאות ואי ספיקת נשימה. יתר על כן, לפלורת החיידקים תפקיד משני. ההשפעה העיקרית היא ההשפעה המרכזית על הריאות, הכוללת ברונכוספזם נרחב, ייצור מוגבר של כיח וריר, איסכמיה של הפרנכימה הריאתית עקב עווית נרחבת של עורקי הריאה הקטנים, מה שמוביל במהירות להפרעות דיסטרופיות, קילוף של האפיתל האלוואולרי וירידה בתפקוד חילוף הגזים של הריאות.
אם זה מלווה בדיכוי רפלקס השיעול, אי ספיקת נשימה מסוג בולברי, אזי נוצרת איום חמור על חיי המטופל. ברוב המקרים, טרכיוברונכיט מוגלתי הנגרם כתוצאה מכך אינו מטופל היטב לטיפול אנטיבקטריאלי ומחמיר את אי הספיקה הנשימתית, אשר משפיעה באופן מיידי על עלייה בהיפוקסיה מוחית. לפיכך, הפרעה של הנשימה החיצונית, אפילו עם פיצוי יחסי על הפרעות מוחיות, עלולה להוביל לתוצאה קטלנית. לעתים קרובות, חולים לאחר תרדמת חוזרים להכרה, אך לאחר מכן מתים מאי ספיקת נשימה גוברת ובצקת מוחית היפוקסית.
שינויים דיסטרופיים מתפתחים במהירות לא רק בריאות, אלא גם בכבד, במערכת העיכול, בבלוטות יותרת הכליה ובכליות. דלקת בדרכי השתן ופצעי לחץ, המתפתחים במהירות בהיעדר טיפול טוב בחולה, מהווים איום על חייו של המטופל. אך ניתן להימנע מסיבוכים אלה אם הרופאים זוכרים אותם ויודעים כיצד להילחם בהם.
בסיכום בחינת הפתוגנזה של קרע ב-AVM, יש להדגיש כי התמותה בדימומים תוך גולגולתיים כאלה נמוכה יותר מאשר בקרע של מפרצות עורקיות ובשבץ מוחי דימומי יתר לחץ דם, אם כי היא מגיעה ל-12-15%. AVM מאופיינים בדימומים חוזרים, לעיתים מרובים, עם מחזוריות משתנה, דבר שאי אפשר לחזות. במקרה של מהלך שלילי של התקופה שלאחר הדימום, המנגנונים הפתוגניים המפורטים עלולים להוביל לתוצאה קטלנית.
תסמינים מום עורקי-ורידי
סוג דימומי של המחלה (50-70% מהמקרים). סוג זה מאופיין בנוכחות יתר לחץ דם עורקי אצל המטופל, גודל קטן של הצומת המום, ניקוז שלו לוורידים עמוקים, מום עורקי-ורידי של גומת הגולגולת האחורית שכיח למדי.
דימום מסוג דימום הוא התסמין הראשון של ביטוי של מום עורקי-ורידי ב-50% מהמקרים, וגורם לתוצאה מפורטת ב-10-15% ונכות ב-20-30% מהמטופלות (נ. מרטין ואחרים). הסיכון השנתי לדימום בחולים עם מום עורקי-ורידי הוא 1.5-3%. הסיכון לדימום חוזר במהלך השנה הראשונה מגיע ל-8% ועולה עם הגיל. דימום ממום עורקי-ורידי הוא הגורם ל-5-12% מכלל תמותת האימהות ול-23% מכלל הדימומים התוך-גולגולתיים בנשים הרות. תמונה של דימום תת-עכבישי נצפה ב-52% מהמטופלות. ב-17% מהמטופלות מתרחשות צורות מורכבות של דימום: היווצרות המטומות תוך-מוחיות (38%), תת-דורליות (2%) ומעורבות (13%), והמוטמפונדה של החדרים מתפתחת ב-47%.
הסוג העייף של המום אופייני לחולים עם מומים עורקיים-ורידיים גדולים הממוקמים בקליפת המוח. אספקת הדם למום העורקי-ורידי מסופקת על ידי ענפים של עורק המוח האמצעי.
התסמינים האופייניים ביותר לסוג הטרפיד הם תסמונת עוויתית (ב-26-27% מהחולים עם מום עורקי-ורידי), כאבי ראש מקבציים וגירעון נוירולוגי מתקדם, כמו בגידולי מוח.
גרסאות של ביטויים קליניים של מומים עורקיים-ורידיים
כפי שכבר צוין, הביטוי הקליני הראשון הנפוץ ביותר של דימום תוך גולגולתי ספונטני (40-60% מהחולים). הוא מתרחש לעיתים קרובות ללא סימנים מוקדמים, בעיצומה של בריאות מלאה. רגעים מעוררי כאב יכולים להיות מאמץ פיזי, מצב לחץ, מתח נוירופסיכי, נטילת מינונים גדולים של אלכוהול וכו'. ברגע קרע ב-AVM, החולים חשים כאב ראש חד פתאומי, כמו מכה או קרע. הכאב גובר במהירות, וגורם לסחרחורת, בחילות והקאות.

אובדן הכרה עלול להתרחש תוך מספר דקות. במקרים נדירים, כאב הראש עשוי להיות קל, המטופלים אינם מאבדים את הכרתם, אך חשים שגפייםיהם נחלשות וקהות (בדרך כלל בצד הנגדי של הדימום), והדיבור נפגע. ב-15% מהמקרים, הדימום מתבטא כהתקף אפילפטי מלא, שלאחריו המטופלים עלולים להישאר במצב של תרדמת.
כדי לקבוע את חומרת הדימום מ-AVM, ניתן להשתמש בסולם האנט-הס שניתן לעיל כבסיס עם כמה התאמות. בשל העובדה שדימומים מ-AVM יכולים להיות בעלי תסמינים שונים מאוד, תסמינים נוירולוגיים מוקדיים יכולים לגבור על תסמינים מוחיים כלליים. לכן, חולים עם רמות תודעה ברמות I או II של הסולם יכולים לסבול מהפרעות נוירולוגיות מוקדיות קשות (המיפרזיס, המיהיפסתזיה, אפזיה, המיאנופסיה). שלא כמו דימומים אנוריזמליים, קרע ב-AVM נקבע לא על ידי חומרת ושכיחות האנגיוספזם, אלא על ידי נפח ומיקום ההמטומה התוך-מוחית.
תסמונת קרומי המוח מתפתחת לאחר מספר שעות וחומרתה עשויה להשתנות. לחץ הדם עולה בדרך כלל, אך לא בצורה חדה ולא למשך זמן רב כמו במקרה של מפרצת עורקית קרועה. בדרך כלל, עלייה זו אינה עולה על 30-40 מ"מ כספית. ביום השני או השלישי מופיעה היפרתרמיה ממקור מרכזי. מצבם של החולים מחמיר באופן טבעי ככל שהבצקת המוחית גוברת ופירוק הדם שנשפך מתעצם. זה נמשך עד 4-5 ימים. עם מהלך חיובי, לאחר התייצבות ביום ה-6-8, מצבם של החולים מתחיל להשתפר. הדינמיקה של תסמינים מוקדיים תלויה בלוקליזציה ובגודל ההמטומה.
במקרה של דימום באזורים תפקודיים חשובים במוח או הרס של מוליכים מוטוריים, תסמיני אובדן מופיעים באופן מיידי ונמשכים זמן רב ללא כל דינמיקה. אם תסמיני אובדן אינם מופיעים באופן מיידי, אלא מתגברים במקביל לבצקת מוחית, ניתן לצפות שהגירעון ישוחזר תוך 2-3 שבועות, כאשר הבצקת תחלוף לחלוטין.
התמונה הקלינית של קרע ב-AVM מגוונת למדי ותלויה בגורמים רבים, העיקריים שבהם הם: נפח ומיקום הדימום, חומרת תגובת הבצקת המוחית ומידת המעורבות של מבני גזע המוח בתהליך.
מומים עורקיים-ורידיים יכולים להתבטא כהתקפים אפילפטיים (30-40%). הגורם להתפתחותם יכול להיות הפרעות במחזור הדם באזורים סמוכים במוח עקב תופעת הגניבה. בנוסף, המום עצמו יכול לגרות את קליפת המוח, וליצור הפרשות אפילפטיות. וכבר דיברנו על סוגים מסוימים של AVM, סביבם מתפתחת גליוזיס של רקמת המוח, שלעתים קרובות מתבטאת גם בהתקפים אפילפטיים.
תסמונת אפילפטית הנגרמת על ידי נוכחות של התקף אפילפטי (AVM) מאופיינת בהופעתה חסרת סיבה בבגרות, לרוב בהיעדר מוחלט של גורם מעורר. התקפים יכולים להיות כלליים או מוקדיים. נוכחות של מרכיב מוקדי ברור בהתקף אפילפטי בהיעדר תסמינים מוחיים כלליים צריכה לעורר את הרעיון של AVM אפשרי. אפילו התקפים כלליים, אם הם מתחילים בעוויתות בעיקר באותן גפיים עם סיבוב מאולץ של הראש והעיניים לצד אחד או אחר, הם לרוב ביטוי של AVM. בתדירות נמוכה יותר, חולים חווים התקפים קלים כגון היעדרויות או הכרה דמדומים. התדירות והמחזוריות של התקפים אפילפטיים יכולות להשתנות: מבודדים ועד חוזרים.
טפסים
VV לבדב ושותפיו למחקר זיהו שלושה וריאנטים של תסמונת מוחית-לבבית על סמך נתוני א.ק.ג.:
- סוג I - הפרה של תפקודי האוטומטיזם והעירור (טכיקרדיה סינוסית או ברדיקרדיה, הפרעות קצב, פרפור פרוזדורים);
- סוג II - שינויים בתהליכי רה-פולריזציה, שינויים חולפים בשלב הסופי של קומפלקס החדרים בהתאם לסוג האיסכמיה, נזק לשריר הלב עם שינויים בגל T ובמיקום מקטע ST;
- סוג III - הפרעת תפקוד הולכה (חסימה, סימנים של עומס מוגבר על הלב הימני). שינויי אק"ג אלה יכולים להיות משולבים וחומרתם תואמת את חומרת המצב הכללי של החולים.
סיבוכים ותוצאות
מום עורקי-ורידי (AVM) הוא אנומליה וסקולרית מולדת שבה עורקים וורידים מחוברים ללא שכבת נימים מתווכת. סיבוכים והשלכות של AVM יכולים להיות חמורים ותלויים בגודל, במיקום ובמאפיינים של המום הספציפי. חלק מהם כוללים:
- שבץ מוחי: אחד הסיבוכים החמורים ביותר של מחלות רקע (AVM) הוא הסיכון לשבץ מוחי. מומים יכולים ליצור מסלולים לא תקינים לזרימת דם, מה שעלול להוביל לדימום במוח ולגרום לשבץ מוחי. שבץ מוחי יכול להיות בעל דרגות חומרה שונות ולהותיר חסרים נוירולוגיים שיוריים.
- אפילפסיה: AVMs עלולים לגרום להתקפים אפילפטיים אצל חלק מהחולים, במיוחד אם המום ממוקם באזורים מסוימים במוח.
- דימום: מומים יכולים להיות בלתי צפויים ולגרום לדימום במוח. זה יכול להיות סיבוך מסכן חיים ולהוביל לתוצאות חמורות.
- הידרוצפלוס: אם ה-AVM ממוקם ליד חדרי המוח, הוא יכול לגרום להידרוצפלוס, מה שעלול להוביל להצטברות נוזלים עודפים במוח ולעלייה בלחץ תוך גולגולתי.
- ליקויים נוירולוגיים: AVM יכול לפגוע ברקמת המוח הסובבת ולגרום למגוון ליקויים נוירולוגיים, כולל שיתוק, הפרעות חושיות ולקיעות בדיבור ובקואורדינציה מוטורית.
- כאב וכאבי ראש: חולים עם AVM עלולים לחוות כאב כרוני וכאבי ראש הקשורים למום.
- השפעות פסיכולוגיות: סיבוכים כתוצאה מ-AVM יכולים להיות בעלי השפעה משמעותית על הרווחה הנפשית של המטופלים, כולל חרדה, דיכאון ולחץ.
- הגבלות על אורח חיים: לאחר גילוי AVM, מטופלים עשויים להזדקק לשינויים באורח החיים והמלצות לניהול סיכונים, כולל הגבלת פעילות גופנית ופעילויות מסוימות.
אבחון מום עורקי-ורידי
אבחון של מום עורקי-ורידי (AVM) כרוך בדרך כלל במגוון בדיקות הדמיה כדי לאשר את קיומו ולהעריך את מאפייני המום. השיטות העיקריות המשמשות לאבחון AVM הן:
- אנגיוגרפיה בתהודה מגנטית (MRA): MRA היא אחת השיטות העיקריות לאבחון גידולים עצביים של כלי הדם (AVMs). זוהי בדיקה לא פולשנית הממחישה את מבנה כלי הדם וזרימת הדם במוח באמצעות שדות מגנטיים וגלי רדיו. MRA יכולה לקבוע את מיקומו, גודלו וצורת האנגיוגרפיה של ה-AVM.
- אנגיוגרפיה דיגיטלית באמצעות חיסור (DSA): זוהי הליך פולשני יותר הכולל הזרקת חומר ניגוד ישירות לכלי הדם דרך קטטר ושימוש בקרני רנטגן כדי לייצר תמונות באיכות גבוהה של כלי הדם במוח. DSA מאפשר בדיקה מפורטת יותר של מבנה ה-AVM ודפוסי זרימת הדם.
- טומוגרפיה ממוחשבת (CT): ניתן להשתמש ב-CT כדי לזהות מחלות רקע (AVM) ולהעריך סיבוכים אפשריים, כגון דימום. במידת הצורך, ניתן להשתמש בחומר ניגוד כדי לשפר את הראייה.
- סריקת דופלקס וסקולרית (אולטרסאונד דופלקס): טכניקה זו עשויה להיות שימושית לבדיקת כלי הדם בצוואר ובראש ולזיהוי הפרעות בזרימת הדם הקשורות לאולטרסאונד דו-וסקולרי.
- ספקטרוסקופיית תהודה מגנטית (MRS): MRS יכולה לספק מידע על ההרכב הכימי של רקמות באזור ה-AVM ולחשוף סימנים לשינויים מטבוליים.
- אקואנצפלוגרפיה: זוהי בדיקת אולטרסאונד בה ניתן להשתמש כדי להעריך את זרימת הדם ואת מבנה המוח.
- טומוגרפיה ממוחשבת אנגיוגרפיה (CTA): CTA משלב CT ואנגיוגרפיה כדי לייצר תמונות תלת-ממדיות של כלי הדם במוח.
לאחר אבחון AVM, חשוב לבצע הערכה מפורטת של מאפייני המום, כגון גודלו, צורתו וחומרתו. הערכה זו תסייע לקבוע האם יש צורך בטיפול ואת אפשרות הטיפול הטובה ביותר, כולל הסרה כירורגית, אמבוליזציה, טיפול בקרינה או השגחה. ההחלטה לטפל ב-AVM צריכה להתקבל בשיתוף פעולה בין המטופל לצוות הרפואי, תוך התחשבות בנסיבות האישיות של כל מקרה ומקרה.
אבחון דיפרנציאלי
אבחנה מבדלת של מומים עורקיים-ורידיים (AVM) יכולה להיות שלב חשוב בהערכת מטופל עם שינויים בכלי הדם במוח. AVMs הן אנומליות בכלי הדם שבהן עורקים וורידים מחוברים ללא שכבת נימים מתערבת. הם יכולים לגרום למגוון תסמינים ומצבים, והבחנה ביניהן מהפרעות כלי דם אחרות חשובה לטיפול נכון. חלק מהמצבים שעשויים לדרוש אבחנה מבדלת עם AVMs כוללים:
- שבץ מוחי: שבץ מוחי יכול לחקות את הסימפטומים של שבץ מוחי AVM, במיוחד אם השבץ נגרם משינויים בכלי הדם. ההבחנה עשויה לדרוש טומוגרפיה ממוחשבת (CT) או דימות תהודה מגנטית (MRI) של המוח כדי להמחיש את השינויים בכלי הדם.
- המטומה: המטומות, כגון המטומה תת-דורלית או אפידורלית, יכולות לחקות תסמיני AVM, במיוחד אם הן מלוות בכאב ראש ותסמינים נוירולוגיים. סריקת CT או MRI עשויה לסייע בקביעת הגורם לתסמינים.
- גידולי מוח: גידולי מוח יכולים לגרום למגוון תסמינים שעשויים להיות דומים לאלה של AVM. האבחון עשוי לכלול MRI עם חומר ניגוד ובדיקות הדמיה אחרות.
- מיגרנה: מיגרנות עם אאורה יכולות לחקות תסמיני AVM, כגון הפרעות ראייה וסחרחורת. היסטוריה רפואית ובדיקות נוספות יכולות לסייע בהבחנה בין השניים.
- דלקת כלי דם מוחית: דלקת כלי דם עלולה לגרום לדלקת בכלי הדם ולמומים בכלי הדם שעלולים לחקות את הסימפטומים של דלקת כלי דם מוחית. ביופסיה או אנגיוגרפיה עשויות לשמש לאבחון דלקת כלי דם.
- פקקת ורידית: פקקות ורידיות יכולות לחקות את הסימפטומים של פקקת ורידית, במיוחד אם ישנה הפרעה בזרימה הוורידית מהמוח. מחקרים נוספים עשויים לסייע בזיהוי פקקת.
לצורך אבחון מבדל מדויק של AVMs, הבדיקה כוללת בדיקה קלינית מקיפה, שיטות נוירו-אדוקטורליות (CT, MRI, אנגיוגרפיה), לעיתים ביופסיה והליכים מיוחדים אחרים בהתאם לתסמינים ולנסיבות הספציפיים.
למי לפנות?
יַחַס מום עורקי-ורידי
הטיפול במום עורקי-ורידי (AVM) תלוי בגודלו, במיקומו, בתסמינים ובסיבוכים הפוטנציאליים. במקרים מסוימים, AVM עשוי להיות קטן ואינסימפטומטי, וייתכן שלא ידרוש טיפול פעיל. עם זאת, אם ישנם תסמינים או סיכון לדימום, טיפול עשוי להיות נחוץ. חלק מהטיפולים עבור AVM כוללים:
- ניתוח: ניתן לשקול הסרה כירורגית של ה-AVM במקרים בהם המום נמצא במיקום נגיש ובעל מורכבות נמוכה. הסרה כירורגית יכולה לסייע במניעת הסיכון לדימום ולהפחית תסמינים. זהו הליך מורכב ועשוי לשאת סיכונים כגון נזק לרקמות ולעצבים הסובבים.
התערבויות פתוחות (טרנסגולגולתיות):
- שלב א' - קרישת דם של צינורות מפרקים;
- שלב II - בידוד ליבת המום העורקי-ורידי;
- שלב III - קשירה וקרישה של הזרימה האפרנטית והסרת המום העורקי-ורידי,
התערבויות אנדווסקולריות:
- חסימה נייחת של עורקי הזנה באמצעות בלון - אמבוליזציה של הזרימה (ללא שליטה);
- שילוב של חסימה זמנית או קבועה באמצעות בלון עם אמבוליזציה של הזרימה;
- אמבוליזציה סופר-סלקטיבית.
מום עורקי-ורידי מטופל גם באמצעות רדיותרפיה (גאמא-נייף, סייבר-נייף, ליטיום-נקז וכו').
- אמבוליזציה: אמבוליזציה היא הליך בו מחדירים חומרים רפואיים או דבק לכלי דם כדי לחסום את זרימת הדם אל ה-AVM. אמבוליזציה יכולה לשמש כשלב הכנה לפני ניתוח או כטיפול עצמאי. היא יכולה לסייע בהפחתת הדימום ואת גודל ה-AVM.
- טיפול בקרינה: טיפול בקרינה עשוי לשמש לטיפול ב-AVM, במיוחד במקרים בהם טיפולים אחרים עשויים להיות מסוכנים מדי. טיפול בקרינה נועד להפחית את הדימום ב-AVM ועשוי לדרוש מספר טיפולים.
- תרופות: במקרים מסוימים, ניתן להשתמש בתרופות כדי להפחית תסמינים כגון כאב או התכווצויות. ניתן להשתמש בתרופות גם כדי לשלוט בלחץ הדם כדי להפחית את הסיכון לדימום.
- תצפית וניהול תסמינים: במצבים מסוימים, במיוחד אם ה-AVM קטן ואינו גורם לתסמינים, ניתן לקבל החלטה פשוט לצפות במצב ולטפל בתסמינים לפי הצורך.
הטיפול ב-AVMs חייב להיות מותאם אישית לכל מטופל, וההחלטה לבחור שיטה תלויה בנסיבות הספציפיות. חשוב לדון בכל אפשרויות הטיפול עם איש מקצוע בתחום הבריאות ולבצע הערכה יסודית של המטופל כדי לקבוע את תוכנית הטיפול הטובה ביותר. תוצאות הטיפול יכולות להיות מוצלחות, והמטופלים יכולים להשיג שיפור או החלמה מלאה, אך כל מקרה הוא ייחודי.
תַחֲזִית
הפרוגנוזה של מום עורקי-ורידי (AVM) תלויה במספר גורמים, כולל גודלו, מיקומו, תסמיניו, גיל המטופל והצלחת הטיפול. חשוב לזכור כי AVM הוא מצב רפואי שיכול להתבטא בצורה שונה אצל מטופלים שונים, והפרוגנוזה עשויה להשתנות מאדם לאדם. להלן מספר היבטים כלליים של הפרוגנוזה של AVM:
- סיכון לדימום: הסיכון העיקרי ל-AVM הוא הסיכון לדימום (הורמוגרפיה) במוח. AVMs קטנים עם סיכון נמוך לדימום עשויים להיות בעלי פרוגנוזה טובה ולא לגרום לבעיות חמורות. עם זאת, AVMs גדולים ובינוניים יכולים להוות סיכון משמעותי.
- תסמינים: תסמינים הקשורים ל-AVM, כגון כאבי ראש, התקפים, שיתוק או הפרעות חושיות, יכולים להשפיע על הפרוגנוזה. במקרים מסוימים, טיפול מוצלח יכול לשפר או לבטל את התסמינים.
- גודל ומיקום: מחלות ריאה (AVM) הממוקמות במקומות מסוכנים יותר, כמו עמוק במוח או ליד מבנים קריטיים, עשויות להיות בעלות פרוגנוזה גרועה יותר. עם זאת, אפילו מחלות ריאה גדולות רבות ניתנות לטיפול בהצלחה.
- טיפול: טיפול ב-AVM עשוי לכלול הסרה כירורגית, אמבוליזציה, טיפול בקרינה או תרופות. טיפול מוצלח יכול להפחית את הסיכון לדימום ולשפר את הפרוגנוזה.
- גיל: גיל המטופל יכול גם הוא להשפיע על הפרוגנוזה. לילדים ולמבוגרים צעירים יש לעיתים קרובות פרוגנוזה טובה יותר מאשר לחולים מבוגרים.
- תחלואה נלווית: נוכחות של מצבים רפואיים אחרים או גורמי סיכון, כגון לחץ דם גבוה או הפרעות דימום, עשויים להשפיע על הפרוגנוזה והטיפול ב-AVM.
חשוב לציין כי AVM דורש ניטור וטיפול רפואיים קפדניים. ההחלטה על שיטת הטיפול והפרוגנוזה צריכה להתקבל על ידי נוירוכירורגים ונוירורדיאולוגים מוסמכים, על סמך הערכה מקיפה של כל מקרה לגופו.

