המומחה הרפואי של המאמר
פרסומים חדשים
גורמים ופתוגנזה של דיפתריה
סקירה אחרונה: 04.07.2025

כל תוכן iLive נבדק מבחינה רפואית או נבדק למעשה כדי להבטיח דיוק עובדתי רב ככל האפשר.
יש לנו קווים מנחים קפדניים המקור רק קישור לאתרים מדיה מכובד, מוסדות מחקר אקדמי, בכל עת אפשרי, עמיתים מבחינה רפואית מחקרים. שים לב שהמספרים בסוגריים ([1], [2] וכו ') הם קישורים הניתנים ללחיצה למחקרים אלה.
אם אתה סבור שתוכן כלשהו שלנו אינו מדויק, לא עדכני או מפוקפק אחרת, בחר אותו ולחץ על Ctrl + Enter.
דיפתריה היא פרדיגמה של מחלות זיהומיות רעילות. בשנת 1883, קלבס הדגים כי Corynebacterium diphtheriae היה הגורם לדיפתריה. שנה לאחר מכן, לופלר גילה שניתן לגדל את האורגניזם רק מחלל האף והלוע והציע שהנזק לאיברים הפנימיים נגרם מרעלן מסיס. עד 1888, רו וירסין הראו שבעלי חיים שהוזרקו להם תסנינים סטריליים של C. diphtheriae פיתחו פתולוגיה של איברים שאינה ניתנת להבחנה מזו של דיפתריה אנושית; זה הוכיח כי אקסוטוקסין חזק היה גורם הארסיות העיקרי.
דיפתריה היא לרוב זיהום בדרכי הנשימה העליונות הגורם לחום, כאב גרון וחולשה. קרום פיברין עבה, אפור-ירוק, שהוא פסאודו-ממברנה, נוצר לעיתים קרובות באתר/י ההדבקה כתוצאה מההשפעות המשולבות של גדילת חיידקים, ייצור רעלים, נמק רקמות בסיסי ותגובת החיסון של הפונדקאי. ההכרה בכך שנזק מערכתי לאיברים נובע מפעולת רעלן הדיפתריה הובילה לפיתוח טיפול יעיל מבוסס נוגדנים לטיפול בזיהום חריף וחיסון טוקסואידי יעיל ביותר.
למרות שחיסון בטוקסואידים הפך את הדיפתריה למחלה נדירה באזורים שבהם תקני בריאות הציבור דורשים חיסון, התפרצויות של דיפתריה עדיין מתרחשות בקבוצות לא מחוסנות ובקבוצות בעלות מערכת חיסון מוחלשת. לעומת זאת, התפרצויות נרחבות של דיפתריה שהגיעו לממדים מגפיים התרחשו באזורים שבהם תוכניות חיסון פעילות הושעו.
סוגים אחרים של קורינבקטריה
בנוסף ל-C. diphtheriae, C. ulcerans ו-C. pseudotuberculosis, C. pseudodiphtheriticum ו-C. xerosis עלולים לעיתים לגרום לזיהומים באף ובעור. שני הזנים האחרונים מזוהים בזכות יכולתם לייצר פיראזינמידאז. ברפואה וטרינרית, C. renale ו-C. kutscheri הם פתוגנים חשובים, הגורמים לפיאלונפריטיס בבקר ולזיהומים סמויים בעכברים, בהתאמה.
גורם ל
הגורם לדיפתריה, Corynebacterium diphtheriae, הוא מוט דק, מעוקל מעט עם עיבויים בצורת אלה בקצוות, ללא תנועה; הוא אינו יוצר נבגים, קפסולות או שוטונים, והוא גרם-חיובי.
בנוסף לרעלן, דיפתריה קורינבקטריה מייצרת במהלך תהליכי חייהם נויראמינידאז, היאלורונידאז, המוליזין, גורמים נמקיים וגורמים מפוזרים, אשר יכולים לגרום לנמק והתנזלות של החומר העיקרי של רקמת החיבור.
בהתבסס על יכולתם ליצור רעלן, חיידקי דיפתריה קורינבקטריה מחולקים לטוקסיגניים ולא רעילים.
רעלן דיפתריה הוא אקסוטוקסין חיידקי חזק הקובע הן את הביטויים הקליניים הכלליים והן את הביטויים הקליניים המקומיים של המחלה. הטוקסיגניות נקבעת גנטית. קורינבקטריות לא טוקסיגניות של דיפתריה אינן גורמות למחלה.
על פי מאפיינים תרבותיים ומורפולוגיים, כל חיידקי הדיפתריה קורינבקטריה מחולקים ל-3 וריאנטים: gravis, mitis, intermedius. אין תלות ישירה של חומרת המחלה בוריאנט של חיידקי הדיפתריה קורינבקטריה. כל וריאנט מכיל זנים טוקסיגניים וזנים לא טוקסיגניים. חיידקי קורינבקטריה טוקסיגניים מכל הוריאנטים מייצרים רעלן זהה. [ 1 ]
מבנה, סיווג וסוגי אנטיגנים
Corynebacterium diphtheriae הוא זן גראם-חיובי, לא נייד, בצורת מוט בצורת אלה. זנים הגדלים ברקמה או בתרביות ישנות יותר במבחנה מכילים נקודות עדינות בדפנות התא המאפשרות דהיית צבע במהלך צביעת גראם ומובילות לתגובת גראם משתנה. תרביות ישנות יותר מכילות לעיתים קרובות גרגירים מטאכרומטיים (פולימטפוספט) הצבועים בכחול-סגול עם כחול מתילן. סוכרים בדופן התא כוללים אראבינוז, גלקטוז ומנוז. בנוסף, ניתן לבודד את האסטר הרעיל 6,6' של טרהלוז, המכיל חומצות קורינמיקוליות וקורינמיקולניות בריכוזים אקווימולריים. מוכרים שלושה סוגי תרביות נפרדים: מיטיס, אינטרמדיוס וגרביס.
רוב הזנים דורשים חומצות ניקוטיניות ופנטותניות לגדילה; חלקם דורשים גם תיאמין, ביוטין או חומצה פימלית. לייצור אופטימלי של רעלן דיפתריה, יש להוסיף חומצות אמינו למצע ולהניחו בצד.
כבר בשנת 1887, תיאר לופלר את בידודם של זנים לא-אלירולנטיים (לא רעילים) של C. diphtheriae, אשר לא היו ניתנים להבחנה מזנים אלימים (רעילים) שבודדו מחולים אצל אנשים בריאים. כיום מוכר כי זנים לא-אלירולנטיים של C. diphtheriae יכולים לעבור להמרה לפנוטיפ אלים לאחר הדבקה וליזוגניזציה על ידי אחד ממספר קורינבקטריופאג'ים שונים הנושאים את הגן המבני לרעלן הדיפתריה, tox. המרה ליזוגנית של הפנוטיפ הלא-אלירולנטי לאלסי יכולה להתרחש הן באתר והן במבחנה. הגן המבני לרעלן הדיפתריה אינו חיוני לא עבור קורינבקטריופאג' ולא עבור C. diphtheriae. למרות תצפית זו, לא נצפתה סחיפה גנטית של רעלן הדיפתריה.
פתוגנזה
נקודות הכניסה לזיהום הן ריריות הלוע, האף, הגרון, ולעתים רחוקות יותר ריריות העיניים ואיברי המין, כמו גם עור פגום, משטחי פצעים או כוויות, תפרחת חיתולים, פצע טבורי שלא נרפא. בנקודת הכניסה, חיידק הדיפתריה קורניבקטריום מתרבה ומפריש אקסוטוקסין.
תרכובת אקסודאט עשירה בפיברינוגן מופרשת ומומרת לפיברין תחת השפעת תרומבוקינאז המשתחררת במהלך נמק של תאי אפיתל. נוצר שכבה פיברינלית - סימן אופייני לדיפתריה.
נשאות אסימפטומטית של האף והלוע נפוצה באזורים אנדמיים לדיפתריה. אצל אנשים רגישים, זנים טוקסיגניים גורמים למחלה על ידי שכפול והפרשת רעלן דיפתריה באף והלוע או בנגעים בעור. נגע הדיפתריה מכוסה לעתים קרובות על ידי ממברנה מדומה המורכבת מפיברין, חיידקים ותאים דלקתיים. רעלן הדיפתריה יכול להתפרק באופן פרוטאוליטי לשני מקטעים: מקטע A N-טרמינלי (תחום קטליטי) ומקטע B (תחומים טרנסממברנליים ותחומים קושרי קולטן). מקטע A מזרז ריבוזילציה של ADP תלוי NAD+ של גורם התארכות 2, ובכך מעכב סינתזת חלבונים בתאים אאוקריוטיים. מקטע B נקשר לקולטן על פני התא ומקל על העברת מקטע A לציטוזול.
חסינות מגנה כוללת תגובת נוגדנים לרעלן דיפתריה לאחר מחלה קלינית או לרעלן דיפתריה (רעלן מומת על ידי פורמלדהיד) לאחר חיסון.
קולוניזציה
מעט ידוע על הגורמים המתווכים את הקולוניזציה של C. diphtheriae. עם זאת, ברור שגורמים אחרים מלבד ייצור רעלן דיפתריה תורמים לאלפיות. מחקרים אפידמיולוגיים הראו כי ליזוטיפ נתון יכול להתקיים באוכלוסייה למשך תקופות ארוכות. מאוחר יותר הוא עשוי להיות מוחלף בליזוטיפ אחר. הופעתו והדומיננטיות שלאחר מכן של ליזוטיפ חדש באוכלוסייה קשורות ככל הנראה ליכולתו להתיישב ולהתחרות ביעילות בפלח שלו בנישה האקולוגית של האף והלוע. Corynebacterium diphtheriae יכול לייצר נוירמינידאז, אשר מפרק חומצה סיאלית על פני התא למרכיביה פירובט וחומצה N-אצטילנויראמינית. גורם קורד (6,6'-di-O-mycoloyl-α, α'-D-trehalose) הוא מרכיב על פני התא של C. diphtheriae, אך תפקידו בקולוניזציה של המארח האנושי אינו ברור.
ייצור רעלי דיפתריה
הגן המבני של רעלן הדיפתריה, tox, שייך למשפחה של קורינבקטריופאג'ים קרובים, שמתוכם ה-β-פאג' הוא הנחקר ביותר. ויסות ביטוי רעלן הדיפתריה מתווך על ידי מדכא המופעל על ידי ברזל, DtxR, המקודד על ידי הגנום של C. diphtheriae. ביטוי רעלן תלוי במצב הפיזיולוגי של C. diphtheriae. בתנאים בהם ברזל הופך למצע המגביל את קצב הגדילה, ברזל מתנתק מ-DtxR, גן הטוקסיקודנדרון מופעל, ורעלן הדיפתריה מסונתז ומופרש למצע הגידול בקצבים מקסימליים.
רעלן הדיפתריה חזק במיוחד; עבור מינים רגישים (למשל בני אדם, קופים, ארנבות, שרקנים) ריכוז נמוך של 100 עד 150 ננוגרם/ק"ג משקל גוף הוא קטלני. רעלן הדיפתריה מורכב משרשרת פוליפפטידית אחת של 535 חומצות אמינו. ניתוח ביוכימי, גנטי וניתוח מבני באמצעות קרני רנטגן מראים כי הרעלן מורכב משלושה תחומים מבניים/תפקודיים:
- ADP-ריבוזילטרנספראז N-טרמינלי (דומיין קטליטי);
- אזור המאפשר מעבר של הדומיין הקטליטי דרך קרום התא (דומיין טרנסממברני);
- תחום קישור קולטנים של תאים אוקריוטיים.
לאחר עיכול ורדוקציה קלים של טריפסין בתנאי דנטורציה, ניתן לפרק באופן ספציפי את רעלן הדיפתריה בלולאה הרגישה לפרוטאז שלו לשני מקטעי פוליפפטיד (A ו-B). מקטע A הוא הרכיב N-טרמינלי בגודל 21 kDa של הרעלן ומכיל את האתר הקטליטי לריבוזילציה של ADP של גורם התארכות 2 (EF-2).
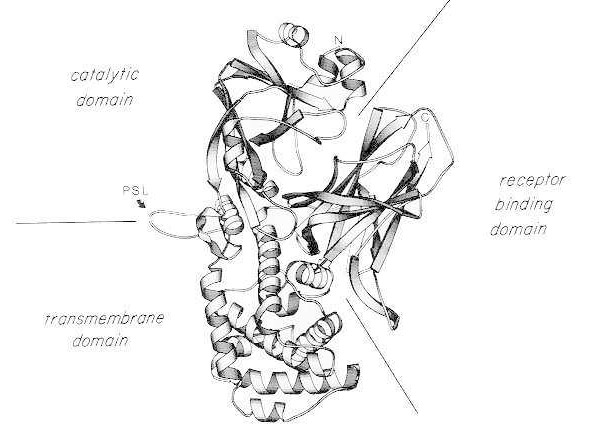
דיאגרמת סרט של מבנה גביש רנטגן של רעלן דיפתריה טבעי מונומרי. (עברה לפי Bennett MJ, Choe S, Eisenberg D: Domain swapping: Entangling aliances between proteins. Proc Natl Acad Sci, USA, 91: 3127, 1994). מוצגים המיקומים היחסיים של הדומיינים הקטליטיים, הטרנסממברנליים והקולטנים. ניתן לחתוך את הרעלן השלם על ידי פרוטאזות דמויות טריפסין ב-Arg190, Arg192 ו/או Arg193, הממוקמות בלולאה הרגישה לפרוטאז (PSL). לאחר חיזור גשר הדיסולפיד בין Cys186 ל-Cys201, ניתן לפרק את הרעלן לשברי A ו-B. מוצגים קצה האמינו (N) והקצה הקרבוקסילי (C) של הרעלן השלם. תרשים הפסים נוצר באמצעות תוכנת MOLESCRIPT.
הפרגמנט C-טרמינלי, פרגמנט B, נושא את הדומיינים הטרנסממברנליים ואת הדומיינים הקושרים לקולטן של הרעלן.
הרעלת תא אאוקריוטי בודד על ידי רעלן דיפתריה כוללת לפחות ארבעה שלבים נפרדים:
- קשירת הרעלן לקולטן שלו על פני התא;
- התקבצות של קולטנים טעונים לתוך בורות מצופים והפנמה של הרעלן באמצעות אנדוציטוזה בתיווך קולטן; לאחר החמצה של שלפוחית האנדוציטים על ידי משאבת פרוטון הקשורה לממברנה, המונעת על ידי ATP,
- החדרת הדומיין הטרנסממברני לתוך הממברנה וסיוע בהעברה של הדומיין הקטליטי לתוך הציטוזול, ו
- ADP-ריבוזילציה של EF-2, וכתוצאה מכך דיכוי בלתי הפיך של סינתזת חלבונים.
הוכח כי מולקולה בודדת של הדומיין הקטליטי המועברת לציטוזול מספיקה כדי להיות קטלנית לתא.
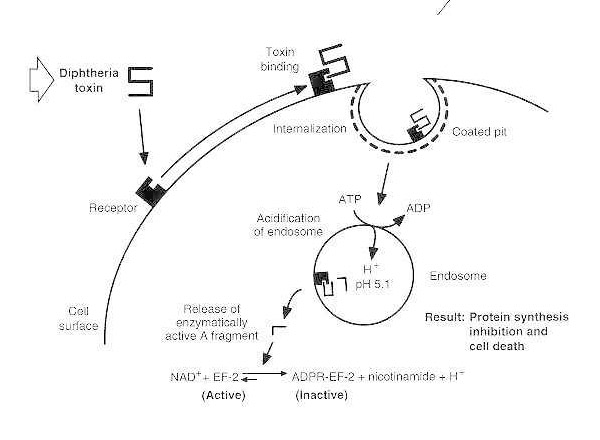
תרשים סכמטי של הרעלת דיפתריה של תא אאוקריוטי רגיש.
הרעלן נקשר לקולטן על פני התא שלו ומועבר לגוף באמצעות אנדוציטוזה בתיווך קולטן; עם החמצת האנדוזום, הדומיין הטרנסממברני מוחדר לקרום השלפוחית; הדומיין הקטליטי מועבר לציטוזול, מה שמוביל לעיכוב סינתזת החלבון ומוות התא.
אֶפִּידֶמִיוֹלוֹגִיָה
לפני החיסון ההמוני של אוכלוסיית ארה"ב בטוקסואיד דיפתריה, דיפתריה הייתה בדרך כלל מחלת ילדות. היבט בולט של חיסון המוני בטוקסואיד דיפתריה הוא שככל שאחוז האוכלוסייה עם רמות חסינות אנטי-רעלן מגנות (≥ 0.01 IU/mL) עולה, תדירות הבידוד של זנים טוקסיגניים מהאוכלוסייה יורדת. כיום, בארצות הברית, שם הדיפתריה הקלינית נעלמה כמעט לחלוטין, בידוד של זנים טוקסיגניים של C. diphtheriae הוא נדיר. מכיוון שזיהום תת-קליני כבר אינו מספק מקור לחשיפה לאנטיגן דיפתריה, ואם לא תוגבר, החסינות לאנטי-רעלן דועכת, לאחוז גדול מהמבוגרים (30 עד 60%) יש רמות נוגדות רעלן מתחת לרמות ההגנה והם נמצאים בסיכון. בארצות הברית, אירופה ומזרח אירופה, התפרצויות אחרונות של דיפתריה התרחשו בעיקר בקרב אנשים המשתמשים באלכוהול ו/או סמים. בתוך קבוצה זו, נשאים של C. diphtheriae טוקסיגני הם בעלי רמה בינונית-גבוהה של חסינות אנטי-רעלן. הפירוק האחרון של אמצעי בריאות הציבור ברוסיה הביא לכך שהדיפתריה הפכה למגפה. עד סוף שנת 1994 דווחו ברוסיה על יותר מ-80,000 מקרים ויותר מ-2,000 מקרי מוות.
התפרצויות מוקדיות של דיפתריה קשורות כמעט תמיד לנשא חיסוני שחזר מאזור שבו דיפתריה אנדמית. ואכן, התפרצויות אחרונות של דיפתריה קלינית בארצות הברית ובאירופה נקשרו למטיילים החוזרים מרוסיה וממזרח אירופה. זנים טוקסיגניים של C. diphtheriae מועברים ישירות מאדם לאדם באמצעות טיפות הנישאות באוויר. ידוע שזנים טוקסיגניים יכולים ליישב ישירות את חלל האף והלוע. בנוסף, הגן הטוקסיגני יכול להתפשט בעקיפין על ידי שחרור קורינבקטריופאג' טוקסיגני וטרנספורמציה ליזוגנית של C. diphtheriae אוטוכתוני לא טוקסיגני in situ. [ 5 ]
בנוסף לקביעת ביוטיפ וליזוטיפ של בידודים של C. diphtheriae, ניתן כיום להשתמש בטכניקות ביולוגיה מולקולרית לחקר התפרצויות דיפתריה. דפוסי עיכול אנדונוקלאזים מוגבלים של DNA כרומוזומלי של C. diphtheriae שימשו לחקר התפרצויות קליניות, כמו גם שימוש ברצפי החדרה משובטים של קורינבקטריאלים כגשש גנטי.
מבחן שיק משמש מזה שנים רבות להערכת חסינות לרעלן דיפתריה, אם כי כיום הוא הוחלף באזורים רבים על ידי הבדיקה הסרולוגית לנוגדנים ספציפיים לרעלן דיפתריה. במבחן שיק, כמות קטנה של רעלן דיפתריה (כ-0.8 ננוגרם ב-0.2 מ"ל) מוזרקת תוך-עורית לאמה (אתר הבדיקה) ו-0.0124 מיקרוגרם של רעלן דיפתריה ב-0.2 מ"ל מוזרק תוך-עורית לאתר הביקורת. הקריאות נלקחות לאחר 48 ו-96 שעות. תגובות עור לא ספציפיות מגיעות בדרך כלל לשיאן לאחר 48 שעות. לאחר 96 שעות, תגובה אדמנתית עם נמק אפשרי באתר הבדיקה מצביעה על חסינות אנטי-רעלית לא מספקת לנטרול הרעלן (≤ 0.03 יחב"ל/מ"ל). דלקת הן באזור הבדיקה והן באזור הביקורת לאחר 48 שעות מצביעה על תגובת רגישות יתר לתכשיר האנטיגן.
טפסים
Corynebacterium diphtheriae מדביק את האף והלוע או את העור. זנים טוקסיגניים מייצרים אקסוטוקסין חזק שיכול לגרום לדיפטריה. תסמיני דיפתריה כוללים דלקת גרון, חום ונפיחות בצוואר או באזור סביב נגע העור. נגעים דיפתריים מכוסים על ידי ממברנה מדומה. הרעלן מתפשט דרך זרם הדם לאיברים מרוחקים ויכול לגרום לשיתוק ואי ספיקת לב. [ 6 ]
ישנם שני סוגים של דיפתריה קלינית: דיפתריה אף-לועית ודיפתריה עורית. תסמיני דיפתריה בלועית נעים בין דלקת גרוע קלה ועד היפוקסיה עקב חסימת דרכי הנשימה על ידי ממברנה מדומה. מעורבות של בלוטות הלימפה הצוואריות עלולה לגרום לנפיחות חמורה של הצוואר (דיפתריה מסוג צוואר השור), והחולה עלול לפתח חום (≥ 103°F). נגעים בעור בדיפטריה עורית מכוסים בדרך כלל על ידי ממברנה מדומה בצבע אפור-חום. סיבוכים מערכתיים מסכני חיים, בעיקר אובדן תפקוד מוטורי (למשל, קושי בבליעה) ואי ספיקת לב, עלולים להתפתח כתוצאה מפעולת רעלן הדיפתריה על נוירונים מוטוריים היקפיים ועל שריר הלב.
לִשְׁלוֹט
בקרת דיפתריה תלויה בחיסון הולם עם טוקסואיד דיפתריה: רעלן דיפתריה מומת על ידי פורמלדהיד, אשר נשאר שלם מבחינה אנטיגנית. הטוקסואיד מוכן על ידי דגירה של רעלן דיפתריה עם פורמלדהיד ב-37 מעלות צלזיוס בתנאים בסיסיים. חיסון דיפתריה צריך להתחיל בחודש השני לחיים עם סדרה של שלוש מנות ראשוניות במרווחים של 4 עד 8 שבועות, ולאחר מכן מנה רביעית כשנה לאחר החיסון הראשוני האחרון. טוקסואיד דיפתריה נמצא בשימוש נרחב כמרכיב בחיסון דיפתריה-שעלת-טטנוס (DPT). מחקרים אפידמיולוגיים הראו כי חיסון נגד דיפתריה יעיל בכ-97%. למרות שחיסון המוני נגד דיפתריה מיושם בארצות הברית ובאירופה ושיעורי החיסון בילדים מספקים, חלק גדול מהאוכלוסייה הבוגרת עשוי להיות בעל טיטר נוגדנים מתחת לרמות המגן. יש לחסן מחדש מבוגרים עם טוקסואיד דיפתריה כל 10 שנים. אכן, יש לתת חיסון דחף בטוקסואיד דיפתריה-טטנוס לנוסעים לאזורים עם שיעורים גבוהים של דיפתריה אנדמית (מרכז ודרום אמריקה, אפריקה, אסיה, רוסיה ומזרח אירופה). בשנים האחרונות, השימוש בתכשירי טוקסואידים מטוהרים ביותר לחיסון צמצם תגובות רגישות יתר קשות מדי פעם. יש לתת חיסון דחף בטוקסואיד דיפתריה-טטנוס לנוסעים לאזורים עם שיעורים גבוהים של דיפתריה אנדמית (מרכז ודרום אמריקה, אפריקה, אסיה, רוסיה ומזרח אירופה). בשנים האחרונות, השימוש בתכשירי טוקסואידים מטוהרים ביותר לחיסון צמצם תגובות רגישות יתר קשות מדי פעם. יש לתת חיסון דחף בטוקסואיד דיפתריה-טטנוס לנוסעים לאזורים עם שיעורים גבוהים של דיפתריה אנדמית (מרכז ודרום אמריקה, אפריקה, אסיה, רוסיה ומזרח אירופה). בשנים האחרונות, השימוש בתכשירי טוקסואידים מטוהרים ביותר לחיסון צמצם תגובות רגישות יתר קשות מדי פעם.
למרות שאנטיביוטיקה (כגון פניצילין ואריתרומיצין) משמשת כחלק מהטיפול בחולי דיפתריה, חיסון פסיבי מהיר עם אנטיטוקסין דיפתריה הוא היעיל ביותר בהפחתת תמותה. זמן מחצית החיים הארוך של אנטיטוקסין ספציפי בזרם הדם הוא גורם חשוב בהבטחת ניטרול יעיל של רעלן הדיפתריה; עם זאת, כדי להיות יעיל, האנטיטוקסין חייב להגיב עם הרעלן לפני שהוא יכול להיכנס לתא.
הנדסה מחדש של רעלן דיפתריה לפיתוח ציטוטוקסינים ספציפיים לקולטנים אאוקריוטיים
הנדסת חלבונים היא תחום חדש ומתפתח במהירות בביולוגיה מולקולרית; היא משלבת מתודולוגיות DNA רקומביננטי וסינתזת DNA בפאזה מוצקה כדי לתכנן ולבנות גנים כימריים שתוצריהם בעלי תכונות ייחודיות. מחקרים על יחסי מבנה-תפקוד של רעלן הדיפתריה הראו בבירור כי רעלן זה הוא חלבון בעל שלושה תחומים: קטליטי, טרנסממברני וקולטן. ניתן היה להחליף גנטית את תחום קישור הקולטן הטבעי של רעלן הדיפתריה בהורמונים וציטוקינים פוליפפטידיים שונים (למשל, הורמון מגרה מלנוציטים α [α-MSH], אינטרלוקין (IL) 2, IL-4, IL-6, IL-7, גורם גדילה אפידרמלי). החלבונים הכימריים או רעלני ההיתוך המתקבלים משלבים את הספציפיות לקישור הקולטן של הציטוקין עם התחומים הטרנסממברניים והקטליטיים של הרעלן. בכל מקרה, רעלני ההיתוך הוכחו כמרעילים באופן סלקטיבי רק את התאים הנושאים את קולטן המטרה המתאים. הראשון מבין רעלני היתוך שעברו שינוי גנטי, DAB 389IL-2, מוערך כעת בניסויים קליניים בבני אדם לטיפול בלימפומות עמידות ובמחלות אוטואימוניות, שבהן תאים עם קולטני IL-2 בעלי זיקה גבוהה ממלאים תפקיד חשוב בפתוגנזה.[ 7 ] מתן DAB 389 IL-2 הוכח כבטוח, נסבל היטב ומסוגל לגרום להפוגה ממושכת של המחלה ללא תופעות לוואי חמורות. סביר להניח שרעלני היתוך מבוססי רעלן דיפתריה יהפכו לחומרים ביולוגיים חדשים וחשובים לטיפול בגידולים או מחלות ספציפיות שבהן ניתן לכוון לקולטנים ספציפיים על פני התא.


 [
[