המומחה הרפואי של המאמר
פרסומים חדשים
ארכנודקטילי
סקירה אחרונה: 04.07.2025

כל תוכן iLive נבדק מבחינה רפואית או נבדק למעשה כדי להבטיח דיוק עובדתי רב ככל האפשר.
יש לנו קווים מנחים קפדניים המקור רק קישור לאתרים מדיה מכובד, מוסדות מחקר אקדמי, בכל עת אפשרי, עמיתים מבחינה רפואית מחקרים. שים לב שהמספרים בסוגריים ([1], [2] וכו ') הם קישורים הניתנים ללחיצה למחקרים אלה.
אם אתה סבור שתוכן כלשהו שלנו אינו מדויק, לא עדכני או מפוקפק אחרת, בחר אותו ולחץ על Ctrl + Enter.
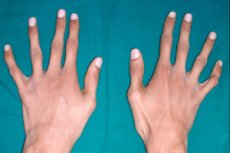
אחת הפתולוגיות התורשתיות הנדירות של רקמת החיבור היא ארכנודקטיליה - עיוות של האצבעות, המלווה בהארכה של העצמות הצינוריות, עקמומיות שלדית, הפרעות במערכת הלב וכלי הדם ובאיברי הראייה.
המחלה תוארה לראשונה על ידי ד"ר וויליאמס והרופא הילדים הצרפתי מרפן, שכינה אותה דוליכוסטנומליה. מאוחר יותר הופיע המונח תסמונת מרפן ברפואה העולמית, ומאז 1902 נעשה שימוש בשם ארכנודקטיליה. הפתולוגיה קשורה להפרעות מולדות של רקמת חיבור, ואחד הסימנים המובילים נחשב לאצבעות "עכביש" מוארכות, דקות ומעוקלות. [ 1 ]
אֶפִּידֶמִיוֹלוֹגִיָה
ארכנודקטיליה נחשבת לפתולוגיה מונוגנית תורשתית של רקמת חיבור, עם תורשה אוטוזומלית דומיננטית, חדירה גבוהה ודרגות שונות של ביטוי.
בכ-75-80% מהמקרים המחלה היא תורשתית, ובמקרים הנותרים היא מתרחשת כתוצאה ממוטציות ספונטניות (בפרט, עקב מוטציות נקודתיות). [ 2 ]
הוכח כי המאפיינים הפתוגניים של ארכנודקטיליה נגרמות על ידי שינויים במספר גנים (ב-95% מהמקרים):
- בגן פיברילין-1 (נחקרו כאלף מוטציות) בכרומוזום 15q21.1;
- הגן TGFβR1 או TGFβR2 על כרומוזום 9 ו-3p24.2-P25.
שינויים אלה משפיעים ישירות על היקף הביטויים הקליניים.
מוטציות בשרשרת α-2 של קולגן מסוג I תוארו ב-5% מהחולים.
שכיחות הארכנודקטיליה היא כ-2 מקרים לכל 5,000 איש. אין קביעה גזעית או מגדרית. [ 3 ]
גורם ל ארכנודקטילי
ארכנודקטיליה מתרחשת כתוצאה ממוטציה ספונטנית. המחלה אינה מאופיינת בסימנים הידועים של פתולוגיות תורשתיות מולדות, ואצבעות מוארכות מתבטאות בעיקר בתסמונת מרפן ובהומוציסטינוריה.
המחלה נדירה, וכל החולים שנמצאו סבלו ממוטציה של הגן FBN1 (גן פיברילין) הממוקם על כרומוזום 15 באזור q21.1. ניתן להסביר את הפולימורפיזם הקליני של התסמונת על ידי מסת המוטציות, כאשר כ-15% מהן הן שינויים מוטציונליים שהתרחשו במהלך ההתעברות. [ 4 ]
זנים לא טיפוסיים של ארכנודקטיליה נגרמים על ידי מוטציות בגנים אחרים: התגלה קשר בין התפתחות הפתולוגיה לבין מוטציות בגן LTBP3, R, הממוקם בכרומוזום 14 באזור q24 ומשנה גורם גדילה.
הרוב המכריע של המוטציות הן מוטציות מסוג missense (כ-57%). יותר מ-20% הן מחיקות קטנות, עם אובדן של חלקים כרומוזומליים, כ-12% הן מוטציות באתר שחבור, 8% הן מוטציות חסרות משמעות, ו-2% הן סידורים מחדש ומחיקות בקנה מידה גדול. [ 5 ]
ארכנודקטיליה חוזית מולדת נגרמת על ידי הפרעה בסינתזה של חומר החלבון פיברילין-2. הבעיה נגרמת על ידי מוטציה בגן FBN2, הממוקם בכרומוזום החמישי באזור q23-q31. כל המוטציות הן בעיקר מוטציות נקודתיות, הגורמות למעבר קודון לקודד לחומצת אמינו אחרת. [ 6 ]
הומוציסטינוריה מתפתחת על רקע חילוף חומרים לקוי של חומצת האמינו החיונית מתיונין. הבסיס לפתולוגיה עשוי להיות אובדן פעילות או ירידה בפעילות של חומרי האנזים הבאים:
- אנזים ציסטתיונין בטא סינתאז (CBS). הפתולוגיה עמידה לוויטמין B6 ומתבטאת בסימנים האופייניים לצורה שאינה תלויה בוויטמין B6 , אולם מתן תכשיר ויטמין B6 אינו מוביל לשיפור.
- אנזים N5, N10 מתילן-טטרהידרופולט רדוקטאז (MTHFR). חומר אנזימטי זה הוא סובסטרט הגורם לדה-מתילציה של הומוציסטאין והפיכתו למתיונין, חומצת אמינו חיונית המהווה מרכיב של חלבונים וחומרים פפטידיים רבים.
- אנזים N5 מתילן-טטרהידרופולט. מדובר בפתולוגיה התלויה בוויטמין B6, המתפתחת עם מחסור בוויטמין B6 .הכנסת תכשיר ויטמין לגוף מאפשרת לשפר את מצבו של המטופל.
- אנזים הומוציסטאין טרנסמתילאז. מתפתח על רקע הפרעות מטבוליות של קובלמין - ויטמין B12.
גורמי סיכון
ארכנודקטיליה היא מחלה גנטית המאופיינת בנזק מערכתי לרקמת החיבור. הפתולוגיה קשורה לשינויים בגן פיברילין 1, הממוקם בזרוע הקצרה של כרומוזום 15 בלוקוס 21.1.
ארכנודקטיליה עוברת בתורשה באופן אוטוזומלי דומיננטי, עם חדירה גבוהה וביטוי משתנה. הפתולוגיה יכולה להתבטא הן בצד הזכרי והן בצד הנקבי.
פתוגנזה
יותר מ-50% ממסת גוף האדם מורכבת מרקמות חיבור, ובפרט השלד, העור, רשת כלי הדם, הלימפה והדם.
תאי רקמת חיבור מיוצגים על ידי פיברובלסטים ותת-הסוגים שלהם: אוסטאובלסטים, כונדרוציטים, קרטובלסטים, אודונטובלסטים, כמו גם מקרופאגים ותאי מאסט.
רקמת חיבור עוברית היא החומר להיווצרות רכיבים קונסטיטוציוניים, גנטיים ואפיגנטיים. מחלות רקמת חיבור משתקפות במידה זו או אחרת על הגוף כולו, על יכולתו התפקודית ועל מבנה הגוף.
בארכנודקטיליה, ישנה החלפה של נוקלאוטידים בגן המכילה מידע מבני על הפפטיד פיברילין-1. חומר חלבוני זה שייך לקבוצת הגליקופרוטאינים, משתתף במערכת המיקרופיברילית ומהווה את הבסיס לסיבים אלסטיים של רקמת חיבור.
הרקמה שומרת על מבנה יציב הודות למטריצה הבין-תאית, המכילה גורמי גדילה רבים המבטיחים התחדשות תאית שיטתית. כלי דם ורצועות גדולים מכילים סיבי אלסטין רבים, שנזקם גורם לתסמינים העיקריים של ארכנודקטיליה.
גורם הגדילה המתמיר β ניזוק באופן משמעותי: צורתו הלא פעילה אינה קשורה, מה שמוביל לעלייה בפעילות הביולוגית של גורם זה.
הפרעות פיבריליות מובילות להיווצרות לא תקינה של סיבים, וכתוצאה מכך אובדן חוזק וגמישות של העור ומבני רקמות חיבור אחרות.
כאשר מבנה הקולגן מופרע, החוליה העיקרית בהמוסטזיס מופרעת.
מומחים מציינים את מעורבותם של חוסר איזון הורמונלי בהופעה ובהתקדמות של אנומליות במבני רקמת החיבור, כולל ארכנודקטיליה. תסמינים טרומבוטיים נקבעים על ידי הפרעות ריאולוגיות - בפרט, שינויים בצמיגות הדם בכלי הדם המותאמים של אזור הברכיוצפלי.
מערכת העיכול מושפעת עקב הפרעות קולגן: נצפות דיסקינזיה היפומוטורית בילארית, בקעים בפתח הוושט של הסרעפת, אנומליות הפטוביליאריות, צורה כרונית של גסטרודואודניטיס "מחוקה", דוליכוזיגמה.
כיצד עוברת תורשת ארכנודקטיליה?
ארכנודקטיליה עוברת בתורשה כתכונה אוטוזומלית דומיננטית, אך יכולה להתרחש גם כתוצאה ממוטציות ספונטניות. כלומר, הפתולוגיה לא בהכרח חייבת להתבטא באחד מקרובי המשפחה הקרובים - למשל, אצל הורים, סבים וסבתות. מוטציות העומדות בבסיס הפתולוגיה יכולות להתגלות באופן אקראי.
תסמינים ארכנודקטילי
ברפואה, מבחינים בין ארכנודקטיליה סמויה לגלויה. בארכנודקטיליה סמויה, קיימים שינויים, אך הם מבודדים ומוגבלים למערכת איברים אחת או שתיים. ארכנודקטיליה גלויה מתבטאת בהפרעות נראות לעין מרובות עם עוצמת תסמינים משתנה. במקרה זה, מצבו של המטופל עשוי להיות יציב יחסית במשך עשרות שנים, או להתקדם בהתמדה, תוך התבטאות ביחס לאיברים ומערכות אחרים.
לעיתים קרובות, ניתן לאתר את תסמונת הארכנודקטיליה בימים הראשונים לאחר לידת התינוק.
הסימן החיצוני העיקרי של ארכנודקטיליה הוא אצבעות דקות ומוארכות, אשר, בשל גידים קצרים, רוכשות עקמומיות אופיינית ודומות לרגלי עכביש.
אצבעות עכביש או ארכנודקטיליה נראות בבירור כמעט מתקופת הילוד. אך הסימן הופך בולט יותר בסביבות גיל שלוש.
מדדי גדילה אופייניים גם הם: ילדים בדרך כלל גבוהים, אמות הידיים והשוקיים ארוכות, הגפיים דקות ולא פרופורציונליות. חוסר הפרופורציה בולט במיוחד במיקום הגבוה של המותניים ופיקות הברכיים. [ 7 ]
הפרעות שלד אחרות כוללות:
- צורת גולגולת צרה ומוארכת (דוליכוצפלית) עם אזור פנים בעל מבנה חריג;
- תצורה בצורת משפך של החזה (מה שנקרא "ציפור");
- עמוד שדרה מעוקל;
- פריקות מפרק ירך מולדות;
- פריקות רגילות של הברך-כתף;
- עקמומיות של עצם העקב;
- תצורות אוסטאופיטים - גידולי עצם;
- רגליים שטוחות;
- התפתחות לא מספקת של שכבת השומן.
סימנים נוספים של ארכנודקטיליה עשויים לכלול:
- קוֹצֶר רְאִיָה;
- לובן העין כחלחל;
- תת-פריקה של העדשה;
- הפרעות בלב ובכלי הדם (מומים בלב, מפרצת אבי העורקים);
- רזון בולט;
- היפר-מוביליות במפרקים;
- שמיים "מקשתים".
ארכנודקטיליה מאופיינת בעצמות צינוריות מוארכות, הגורמות לעקומות שלדיות שונות. בנוסף, לחולים רבים יש הפרעות פירמידליות, אסימטריה של רפלקסים של גידים, אנוסוקוריה וניסטגמוס על רקע התפתחות שכלית תקינה.
אם אנחנו מדברים על ארכנודקטיליה, המלווה בהומוציסטינוריה, אז המטופל עשוי לחוות את התסמינים הבאים:
- התקפי עוויתות תקופתיים;
- גלאוקומה משנית עם תת-פריקה של העדשה;
- היפרדות רשתית, אסטיגמציה;
- נזק לגזעי עורקים (כולל כליות, מוח);
- אוסטאופורוזיס;
- פַּקֶקֶת;
- פיגור שכלי.
ארכנודקטיליה אצל יילודים
ברוב המקרים, ניתן לזהות ארכנודקטיליה אצל ילד בימים הראשונים לחייו. עם זאת, עם הגיל, התסמינים נוטים להחמיר.
הסימנים הראשונים המאפשרים לחשוד במחלה הם בדרך כלל הבאים:
- גפיים ואצבעות ארוכות באופן יוצא דופן;
- תת משקל במצב גופני תקין של הילד;
- פנים מוארכות וארוכים;
- חוסר שומן בגוף, שרירים מפותחים בצורה גרועה;
- גמישות יתר של המפרקים.
בערך מגיל ארבע, על רקע ארכנודקטיליה, החזה מתחיל להשתנות, עמוד השדרה מתעקם, ומתפתחות רגליים שטוחות.
מבחינת איברי הראייה, נצפים קוצר ראייה, אקטופיה של העדשה, שינויים בקונפיגורציה של הקרנית, פזילה, תהליכים היפופלסטיים בקשתית וברשתית. הפרעות כאלה ניתן להבחין בהן כבר ב-2-3 השנים הראשונות לחייו של ילד, אם כי הן מתקדמות עם השנים.
הסכנה הגדולה ביותר נשקפת מהפרעות במערכת הלב וכלי הדם. אם הפרעות כאלה קיימות, אז בהיעדר טיפול מתאים קיים סיכון גבוה למוות של המטופל כבר בילדות. בין הפתולוגיות המסוכנות במיוחד ניתן להבחין בנזק לדפנות כלי הדם, מומים לבביים, פגמים בכלי הדם הכליליים. לעיתים, אצל ילדים בשנה הראשונה לחייהם, כבר מתגלה אי ספיקת לב גוברת.
ארכנודקטיליה עשויה להיות מלווה בנזק לאיברים אחרים, בפרט, מערכת העצבים, הסמפונות והריאות, העור ומערכת גניטורינארית. הפרעות כאלה מתגלות במהלך הליכי אבחון.
סיבוכים ותוצאות
תופעות הלוואי הנפוצות ביותר של ארכנודקטיליה הן נזק ללב ולאיברי הנשימה. בנוסף, מופיעות בעיות ראייה, עד כדי אובדן ראייה.
חולים עם ארכנודקטיליה דורשים טיפול מורכב בכל הפתולוגיות הקיימות. אם טיפול כזה לא מתבצע, תוחלת החיים של החולים מצטמצמת משמעותית: חולים נדירים ללא התערבות רפואית מצליחים לחיות עד גיל 40. עם השנים, בעיות במערכת הלב וכלי הדם מחמירות, הסיכון לדימומים נרחבים עם תוצאה טרגית עולה.
אנשים הסובלים מארכינודקטיליה צריכים לעבור בדיקות סדירות ולטפל בפתולוגיות נלוות: רק במצב זה יש להם כל סיכוי לחיות חיים ארוכים ללא סיבוכים חמורים.
תסמונת מרפן וארכנודקטיליה דורשות תשומת לב מיוחדת אם החולה נכנסת להריון. במצב כזה, חשוב לבדוק את החולה באופן קבוע ויסודי, ולתמוך רפואית במצב מערכת הלב וכלי הדם שלה. זוהי הדרך היחידה להבטיח הריון מוצלח ולידה בטוחה של הילד.
כדי להימנע מתופעות לוואי שליליות, יש לבדוק באופן קבוע חולים עם ארכנודקטיליה על ידי רופאים, למנוע התפתחות של פתולוגיות לב וכלי דם ושלד. מומלץ להם לנהל אורח חיים בריא בלבד, עם פעילות גופנית מתונה.
אבחון ארכנודקטילי
אבחון קליני של ארכנודקטיליה כולל איסוף תלונות, היסטוריה משפחתית, הערכת פנוטיפ, וכן בדיקות אנתרופומטריות ופיזיות. חשוב לקבוע את נוכחותן של ביטויים של פתולוגיות של רקמת חיבור אצל קרובי משפחה ישירים: לשם כך, מתבצע מחקר גנאלוגי. [ 8 ]
אבחון מעבדתי לארכנודקטיליה כרוך בלימוד מצבם של סוגים מסוימים של רקמת חיבור, המיוצגת על ידי רקמת עצם וסחוס, דם ולימפה. האינפורמטיבי ביותר נחשב למחקר של רמות האוקסיפרולין והגליקוזאמינוגליקנים בנפח השתן היומי. בנוסף, נבדקת תכולת הליזין, הפרולין והאוקסיפרולין בדם. כדי לקבוע יחסים משתנים של סוגים שונים של קולגנים וחריגות מבניות של סיבי קולגן, נקבעת טיפוס בשיטת אימונופלואורסצנציה עקיפה באמצעות נוגדנים פוליקלונליים לקולגן ופיברונקטין. [ 9 ] בהתאם לאינדיקציות, מבוצעות הבדיקות הבאות כדי לשקף את איכות התהליכים המטבוליים של רקמת החיבור:
- גליקוזאמינוגליקנים, פיברילין, פיברונקטין;
- מחקר של הידרוקסיפרולין, סמנים של ביוסינתזה של קולגן מסוג 1, פרופפטידים אמינוטרמינליים של פרוקולגן מסוג 1, סמנים של פירוק קולגן מסוג 1, גלקטוסילוקסיליזין, דאוקסיפירידינולין;
- ניתוח של ויסות מטבוליזם של קולגן (מחקר של מטאלופרוטאינאזות מטריקס ומעכבי רקמות של מטאלופרוטאינאזות מטריקס, גורם גדילה טרנספורמטיבי);
- ניתוח של מיקרו- ומקרו-אלמנטים (תכולת סידן ומגנזיום, זרחן, ברזל, גופרית ונחושת, קובלט וסלניום, אבץ ומנגן, פלואור ונדיום, סיליקון ובורון);
- מחקר של סמנים של היווצרות רקמת עצם וקצב תהליכי שיפוץ (ניתוח תכולת אוסטאוקלצין, פוספטאז אלקלי של העצם, הורמון פאראתירואיד, הורמון סומטוטרופי, פרולקטין, ויטמין D3 , פנטוזידין, הומוציסטאין בשתן ובדם).
אבחון אינסטרומנטלי שואף לזהות פגמים התפתחותיים קיימים ולהעריך את המצב התפקודי של איברים ומערכות. הפרעות לב וכלי דם בארכנודקטיליה דורשות הכללה חובה ברשימת האבחון של הליכים כגון:
- אלקטרוקרדיוגרפיה;
- ניטור א.ק.ג. 24 שעות ביממה;
- בדיקת אולטרסאונד של הלב וכלי הדם.
אנומליות בכלי הדם נבדקות באמצעות טומוגרפיה ממוחשבת או דימות תהודה מגנטית. הליכים אבחנתיים נוספים עשויים לכלול:
- אולטרסאונד של איברי הבטן, מערכת גניטורינארית;
- צילום רנטגן של איברי בית החזה, מפרקי הירך; [ 10 ]
- CT או MRI של עמוד השדרה.
לאחר כל הבדיקות הנדרשות, המטופל מופנה לייעוץ גנטי.
אבחון דיפרנציאלי
קיים דמיון פנוטיפי בין תסמונת בילס לארכנודקטיליה בתסמונת מרפן (מוטציות של הגנים FBN2 ו-FBN1, בהתאמה), הנובע מהזהות הכמעט מלאה של חומרי החלבון פיברילין 1 ופיברילין 2. אין זה מפתיע שהשם השני של תסמונת בילס הוא ארכנודקטיליה של התכווצות. [ 11 ]
בידול מתבצע גם עם פתולוגיות אחרות של רקמת חיבור:
- תסמונת סטיקלר;
- תסמונת אהלרס-דנלוס;
- הומוציסטינוריה;
- ארתרוגרוזיס.
תסמונת בילס מאופיינת בפנוטיפ מרפנואידי, התכווצויות כיפוף מולדות של מפרקים גדולים וקטנים, ארכנודקטיליה של שורש כף היד והרגל, עקמומיות של עמוד השדרה וצורת אוזניים חריגה (מה שנקרא אוזניים "מקומטות"). ניתוח מולקולרי של הגן FBN2 מבוצע כדי לאשר את האבחנה.
ארתרוגרוזיס מאופיינת בכיווצי מפרקים מרובים, קומה נמוכה וירידה באינטליגנציה. צורת האצבעות והאוזניים אינה יוצאת דופן. [ 12 ]
תסמונת אהלרס-דנלוס מאופיינת בקיפוסקוליוזיס, עקמומיות משפכת של החזה, כפות רגליים שטוחות בולטות ושבירה לקויה. ניידות מוגברת ופריקות מפרקים, גמישות גבוהה של העור ורגישות אופייניים.
תסמונת סטיקלר מאופיינת בשינויים בנפח ובנוקשות המפרקים.
למי לפנות?
יַחַס ארכנודקטילי
ארכנודקטיליה היא פתולוגיה גנטית, וכיום אין לרפואה שיטות לתיקון פגמים גנטיים. לכן, הטיפול מכוון לייעל את מצבו של המטופל, למנוע החמרה של הפתולוגיה ולחסל ביטויים סימפטומטיים. נקבע טיפול מורכב, הכולל מספר מומחים רפואיים בו זמנית, בהתאם לסוג התסמינים הבולטים ביותר: לעתים קרובות יש צורך לפנות בנוסף לאורתופד, קרדיולוג, רופא עיניים, גסטרואנטרולוג ורופאים בעלי התמחויות אחרות. [ 13 ]
בין ההמלצות לטיפול קליני בחולים, העקרונות הבאים נחשבים לעקרונות כלליים:
- הגבלת פעילות גופנית, אך לא ביטולה לחלוטין (כחלק מתמיכה במערכת הלב וכלי הדם);
- טיפול תרופתי;
- במידת הצורך - תיקון כירורגי של האזורים הנפגעים ביותר בלב ובכלי הדם;
- תיקון אורתופדי;
- טיפולי ספא, פיזיותרפיה, פעילות גופנית טיפולית.
תזונתם של חולים עם ארכנודקטיליה צריכה לכלול כמות מספקת של מוצרים עתירי חלבון מועשרים במיקרו-אלמנטים, ויטמינים וחומצות שומן. מומלץ לאכול בשר, דגים, פירות ים, שעועית ואגוזים. אם ארכנודקטיליה נגרמת על ידי הומוציסטינוריה, אזי צריכת חלבון מן החי מוגבלת בחדות.
לילדים בעלי מבנה גוף רזה וגבוה מומלץ להכניס לתזונה שלהם שמן זרעי כותנה וסויה, גרעיני חמניות, שומן חזיר ושומן חזיר מגיל צעיר. בנוסף, הם מציעים תכשירים המכילים חומצות שומן רב בלתי רוויות כמו אומגה, אשר מעכבות את ייצור ההורמון הסומטופרוני.
כדי לנרמל את חילוף החומרים של חלבונים, נקבעים ויטמינים מקבוצת B. ניתן להשיג אותם גם ממוצרי מזון: כוסמת, אפונה, כבד.
חשוב מאוד שחומצה אסקורבית תיכנס לגוף המטופל עם המזון. לשם כך, חליטת ורד בר, פלפלים, כרוב, פירות הדר, כמו גם אשחר ים וכרישה כלולים בהכרח בתזונה.
במידת הצורך, מוצע למטופלים תיקון אורתופדי, הנחוץ להפחתת העומס על עמוד השדרה והמפרקים. לשם כך משתמשים בנעליים אורתופדיות, ברכיים ואביזרים אחרים, מדרסים ותחבושות אלסטיות.
טיפול כירורגי מתבצע על פי האינדיקציות.
תרופות
טיפול תרופתי בארכנודקטיליה מתבצע 1-2 פעמים בשנה, בהתאם למצבו של המטופל ולחומרת התסמינים הפתולוגיים. משך הטיפול נקבע באופן אישי והוא בממוצע 4 חודשים. [ 14 ]
כדי לעורר היווצרות קולגן, נקבעות התרופות הבאות: Piaskledin 300, L-lysine או L-proline בשילוב עם תכשירים מולטי ויטמינים מורכבים המכילים חומצה אסקורבית, ויטמיני B, טוקופרול, מגנזיום, אבץ, סלניום, נחושת.
בין כונדרופרוטקטורים, השימוש האופטימלי ביותר הוא כונדרויטין סולפט וגלוקוזאמין סולפט - תרופות המשתתפות בוויסות חילוף החומרים של כונדרוציטים, דיכוי סינתזת אנזימים, הגברת הרגישות של כונדרוציטים לפעולה אנזימטית, גירוי תהליכים אנביליסטיים וכו'. סוכנים משולבים נחשבים אופטימליים לתרופות כאלה: Teraflex, Arthroflex, Arthra וכו'.
מטבוליזם מינרלי מגורה על ידי תרופות המנרמלות תהליכי זרחן-סידן. התרופות המועדפות הן לרוב צורות פעילות של ויטמין D: אלפא D3 טבע, אוקסידוויט, בונוביה וכו'. במקביל, משתמשים בתכשירים של זרחן, סידן ומגנזיום. במהלך הטיפול, רמת הסידן והזרחן בדם או בשתן נבדקת בערך פעם ב-20 יום, ובדיקת דם לפוספטאז אלקליין מבוצעת.
כדי לשפר את המצב הביו-אנרגטי של הגוף, ניתן לרשום פוספדן, ריבוקסין, לציטין, אלקר, קואנזים Q10.
משטר טיפול משוער עשוי להיראות כך:
- כונדרופוטקטור במינון המתאים לגיל, נלקח עם אוכל וכמות מספקת של מים. משך טיפול אחד הוא 3-4 חודשים.
- L-פרולין במינון של 500 מ"ג (לילדים מגיל 12 ומבוגרים) נלקח חצי שעה לפני הארוחות, 1-2 פעמים ביום, במשך שישה שבועות. במידת הצורך, ניתן לרשום בנוסף קומפלקס חומצות אמינו - L-פרולין, L-ליזין, L-לאוצין בכמות של 10-12 מ"ג / קילוגרם משקל. הנטילה מתבצעת 1-2 פעמים ביום, במשך חודשיים.
- תכשירים מורכבים של ויטמינים ומינרלים, סנטרום, או ויטרום, או יוניקאפ, במינון תוך התחשבות בגיל. משך הנטילה הוא 4 שבועות.
משטר טיפול זה מתאים אם חולה עם ארכנודקטיליה מתלונן על בעיות במערכת השרירים והשלד, ותוצאות הבדיקה מצביעות על הפרשה מוגברת של גליקוזאמינוגליקנים בבדיקת שתן יומית ורמות נמוכות של חומצות אמינו חופשיות בדם.
ככלל, הטיפול מתקבל היטב על ידי המטופלים, ללא תופעות לוואי מיוחדות. אם מתגלות תגובות רגישות יתר, התרופות מוחלפות ומשטר הטיפול מותאם.
טיפול פיזיותרפיה
טיפולים פיזיותרפיים לארכנודקטיליה נקבעים בהתאם לאינדיקציות. לדוגמה, במקרה של אוסטאוגנזה לא מספקת, לשיפור הריפוי של שברים בעצמות, או במקרה של סימני אוסטאופורוזיס, מומלץ לבצע אלקטרופורזה עם 5% סידן כלורי, 4% מגנזיום גופרתי, 2% נחושת גופרתי או 2% אבץ גופרתי.
אם מתגלות הפרעות צמחיות-וסקולריות, משתמשים ב-1% נתרן קפאין בנזואט, אפדרין הידרוכלוריד או מזטון.
כדי להפעיל את תפקוד קליפת האדרנל, נקבעים אלקטרופורזה תרופתית עם 1.5% אתימיזול וטיפול דצימטר לאזור האדרנל. [ 15 ]
כדי לייצב את טונוס כלי הדם, מומלץ להשתמש בהליכי מים המקדמים "התעמלות" בכלי הדם. אמבטיות כגון פחמן דו-חמצני, אורן, כלוריד-מימן, מימן גופרתי ורדון מצוינות. נהוגים אמבטיות עיסוי, שטיפה, מקלחות ניגודיות, אמבטיות קצף ומלח.
כדי לשפר את מצב רקמת הסחוס, משתמשים בטיפול מגנטי, אינדוקציה, טיפול בלייזר ואלקטרופורזה עם דימתיל סולפוקסיד (Dimexide).
טיפול כירורגי
ניתוחים לארכנודקטיליה נקבעים אך ורק על פי האינדיקציות. לדוגמה, אם מתגלות הפרעות המודינמיות חמורות על רקע צניחת מסתמים, מבוצעות מפרצת מסיבית של אבי העורקים, החלפת מסתם ופגיעה במקטע אבי העורקים. [ 16 ]
אם ישנן הפרעות תפקודיות בולטות של מערכות הנשימה והלב וכלי הדם הנובעות כתוצאה מעקומות חמורה של בית החזה, מבוצעת ניתוח חזה.
במקרה של תסמונת כאב מתקדמת הנגרמת על ידי עקמת חמורה של 3-4 מעלות, מומלץ גם להתערב כירורגית. מנקודת מבט אופתלמולוגית, אינדיקציות מוחלטות להסרת עדשה הן תת-פריקה של העדשה המסובכת על ידי גלאוקומה משנית, כמו גם קטרקט ושינויים ניווניים ברשתית עם סיכון גבוה להיפרדות.
כל ניתוח בחולים עם ארכנודקטיליה והפרעות אחרות המשפיעות על מבני רקמת החיבור מתבצע רק בשלב של הקלה קלינית וביוכימית יחסית. לאחר ההתערבות, נדרשת השגחה רפואית ארוכת טווח וטיפול אינטנסיבי בתרופות המשפרות את חילוף החומרים של רקמת החיבור.
מְנִיעָה
ארכנודקטיליה היא פתולוגיה גנטית נדירה. לעיתים היא מתרחשת באופן ספונטני אצל הורים בריאים לכאורה. לכן, קשה מאוד מאוד למנוע את המחלה מראש.
אם לאחד ההורים הפוטנציאליים יש היסטוריה משפחתית עמוסה - כלומר, ידוע שמישהו במשפחה סבל מארכינודקטיליה - אז בני הזוג צריכים לפנות לגנטיקאי ולעבור בדיקה גנטית בשלב תכנון ההיריון. לאחר אישור ההריון, הרופא מבצע אבחון טרום לידתי, הכולל בדיקת אולטרסאונד של העובר ומספר בדיקות ביוכימיות:
- בדיקת דם של האם;
- ניתוח מי שפיר;
- דגימת סיסי כוריוני;
- ניתוח של תאי שליה ודם חבל הטבור.
חולים עם ארכנודקטיליה נמצאים תחת מעקב רפואי לאורך כל חייהם. אמצעי מניעה בחולים נועדו למנוע סיבוכים. לשם כך, מתבצע תיקון כירורגי לבבי, נקבע טיפול תרופתי כדי למנוע את הסיכון להיווצרות פקקת. קורסי טיפול אנטיביוטי ניתנים מעת לעת.
תַחֲזִית
הפרוגנוזה לחיי חולי ארכנודקטיליה נקבעת בעיקר על ידי חומרת ההפרעות הנלוות - בפרט, מחלות של מערכת הלב וכלי הדם, מערכת השרירים והשלד ואיברי הראייה. לרוב, הפתולוגיה מסתבכת על ידי קרע ודיסקציה של אבי העורקים. יש לקחת זאת בחשבון ולבצע תיקון ניתוחי לב בזמן, אשר יסייע להאריך את חיי המטופל ולשפר את איכותם.
אם האבחון נעשה בזמן, אז אם המלצות הרופא יבוצעו, ניתן לכנות את הפרוגנוזה חיובית בתנאי. תמיכה רפואית מקלה משמעותית על מהלך הארכנודקטיליה, ולחולים יש הזדמנות לחיות חיים נורמליים ומלאים יחסית מבלי לפתח סיבוכים חמורים.

