המומחה הרפואי של המאמר
פרסומים חדשים
עמילואידוזיס של הכבד
סקירה אחרונה: 29.06.2025

כל תוכן iLive נבדק מבחינה רפואית או נבדק למעשה כדי להבטיח דיוק עובדתי רב ככל האפשר.
יש לנו קווים מנחים קפדניים המקור רק קישור לאתרים מדיה מכובד, מוסדות מחקר אקדמי, בכל עת אפשרי, עמיתים מבחינה רפואית מחקרים. שים לב שהמספרים בסוגריים ([1], [2] וכו ') הם קישורים הניתנים ללחיצה למחקרים אלה.
אם אתה סבור שתוכן כלשהו שלנו אינו מדויק, לא עדכני או מפוקפק אחרת, בחר אותו ולחץ על Ctrl + Enter.
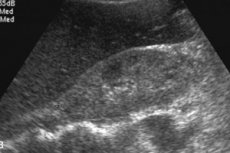
עמילואידוזיס היא בדרך כלל פתולוגיה כללית וסיסטמית המאופיינת בהצטברות של עמילואיד (גליקופרוטאין ספציפי) ברקמות ובעקבות שיבוש תפקוד תקין של איברים. עמילואידוזיס בכבד שכיח הרבה פחות מכליות וטחול [ 1 ] אך כמעט תמיד מלווה בנזק מערכתי לגוף. אף אחת מטכניקות ההדמיה הקיימות אינה יכולה להדגים באופן ספציפי את נוכחותו של עמילואיד. גם כאשר קיים חשד קליני ורדיולוגי, אבחון עמילואידוזיס תלוי בביופסיה של רקמה כדי לאשר את נוכחותם של משקעי עמילואיד. [ 3 ] הטיפול מורכב, מקיף וכולל אמצעים מדכאי חיסון וסימפטומטיים. במקרים חמורים, ייתכן שיהיה צורך בהשתלת כבד.
אֶפִּידֶמִיוֹלוֹגִיָה
הצלחת הטיפול תלויה ישירות באבחון בזמן של המחלה, הגורמת להיווצרות קומפלקס חלבון-פוליסכריד (עמילואיד) באיברים שונים ובכבד. כפי שמראה בפועל, קשה להניח או לחשוד בעמילואידוזיס, אם כי ניתן לזהות ולאשר אותה. העובדה היא שבמעל 80% מהמקרים הלא מזוהים, המחלה מוסתרת קלינית על ידי פתולוגיה בכבד. שיטת האבחון היעילה ביותר היא ביופסיה.
עמילואידוזיס בכבד היא בעיה נדירה יותר בהשוואה לעמילואידוזיס בכליות. יחד עם זאת, כל מקרי הנגעים בכבד מלווים בנגעים באיברים אחרים. לרוב, הפתולוגיה משפיעה בעיקר על חלקים מבניים של השלישייה הכבדית, אשר קובעת את המינימום והאי-ספציפיות של הסימפטומים. התמונה הקלינית והמורפולוגית של חסר הפטוצלולרי ויתר לחץ דם פורטלי מתבטאת בפתולוגיה מסוג מפושט ואינטרא-אונתי.
ביופסיה של כבד מוצדקת כאשר קיימת הפטומגליה ללא תסמינים כבדיים קודמים ובהיעדר תסמונת נפרוטית.
מעורבות מפושטת של הכבד נצפית בכ-25% מהמקרים, וב-75% מהחולים רק דרכי הפורטל מושפעות.
עמילואידוזיס ראשוני משפיע על הכבד ב-90% מהמקרים, בעוד שעמילואידוזיס משני משפיע על הכבד רק ב-47% מהמקרים.
מעורבות בודדת של הכבד היא נדירה ביותר. הכליות (כ-93% מהמקרים), הטחול (72%), הלב (57%), הלבלב (36%), בלוטות יותרת הכליה (29%), המעיים והריאות (21% כל אחד) מושפעים בדרך כלל במקביל.
נשים חולות במחלה כמעט פי שניים מגברים. תוחלת החיים הממוצעת של חולי עמילואידוזיס היא 52-64 שנים.
גורם ל של עמילואידוזיס בכבד
עמילואידוזיס מתרחשת עם היווצרות והצטברות של קומפלקס פוליסכריד-חלבון מורכב - עמילואיד - ברקמת הכבד. בעיית הופעת הנגע הראשוני עד כה אינה נחקרה מספיק. באשר לפתולוגיה משנית, הופעתה קשורה בדרך כלל למחלות כאלה:
- תהליכים זיהומיים כרוניים (שחפת, עגבת, אקטינומיקוזיס);
- תהליכים דלקתיים מוגלתיים (אנדוקרדיטיס מיקרוביאלית, אוסטאומיאליטיס, מחלת ברונכיאקטזה וכו');
- מחלות ממאירות (לוקמיה, סרטן בטני, לימפוגרנולומטוזיס).
הצורה הריאקטיבית של עמילואידוזיס נמצאת בחולים עם טרשת עורקים במקביל, מחלות ראומטולוגיות (מחלת בכטרו, דלקת מפרקים שגרונית), פסוריאזיס, דלקות כרוניות ותהליכים רב-מערכתיים (כולל סרקואידוזיס). גורמי הסיכון העיקריים: נטייה תורשתית, הפרעות בחסינות תאית, היפרגלובולינמיה.
פתוגנזה
ישנן מספר הנחות בנוגע למקור עמילואידוזיס בכבד. רוב המומחים דבקים בגרסה של דיספרוטאינוזיס, באופי האימונולוגי והמוטציוני של המחלה, כמו גם בגנזה תאית מקומית. גרסת הגנזה התאית כוללת שינויים בתגובות הפועלות ברמה התאית (היווצרות של קודמי עמילואיד סיביים על ידי קומפלקס של מקרופאגים), אם כי עמילואיד נוצר ומצטבר מחוץ למבנים התאיים.
גרסת הדיספרוטאינוזיס מבוססת על העובדה שעמילואיד הוא תוצר של מטבוליזם לא תקין של חלבונים. הקשר הפתוגנטי הבסיסי לבעיה טמון בדיספרוטאינמיה והיפרפיברינוגנמיה, המובילות להצטברות של חלבון גס מפוזר ושברים של פרפרוטאינים בפלזמה.
על פי הגרסה האימונולוגית, היווצרות עמילואיד נגרמת על ידי תגובה אנטיגן-נוגדן, שבה תוצרי ריקבון רקמות או חלבונים זרים משמשים כאנטיגנים. הצטברות עמילואיד נמצאת בעיקר באזור היווצרות הנוגדנים ונוכחות מוגזמת של אנטיגנים.
הגרסה הסבירה ביותר, מדענים שוקלים את תיאוריית המוטציה, אשר לוקחת בחשבון מגוון גורמים מוטגניים שיכולים להוביל לחריגות בסינתזת חלבונים.
עמילואיד הוא היפופרוטאין מורכב המורכב מחלבונים כדוריים וסיביים בשילוב עם פוליסכרידים. הצטברות עמילואיד משפיעה על האינטימה והאדווענטיטיה של רשת כלי הדם, על הסטרומה של איברים פרנכימטיים, על מבנה הבלוטות וכו'. הצטברות עמילואיד אינה גורמת נזק תפקודי. הצטברות קטנה אינה גורמת להפרעות תפקודיות, אך עם נוכחות עמילואיד חזקה בכבד, הנפח עולה, המראה של האיבר משתנה, ומתפתח חוסר תפקוד.
עמילואידוזיס בכבד מאופיינת בהצטברות של סיבי עמילואיד בחלל דיס, שבדרך כלל מתחילה באזור הפריפורטלי, אם כי לעיתים היא צנטרילובולרית ויכולה להצטבר גם בכלי הדם של הכבד. [ 4 ], [ 5 ] במקרים חמורים, הצטברות עמילואיד מובילה לאטרופיה של לחץ של הפטוציטים, המונעת את מעבר המרה, וכתוצאה מכך כולסטזיס, או עלולה לחסום את הסינוסואידים, וכתוצאה מכך יתר לחץ דם פורטלי. [ 6 ], [ 7 ], [ 8 ]
תסמינים של עמילואידוזיס בכבד
התמונה הקלינית בעמילואידוזיס בכבד היא מגוונת, תלויה בעוצמת הצטברות העמילואיד, במאפיינים הביוכימיים שלו, במשך התהליך הפתולוגי, במידת הנזק לאיברים ובהפרת מצבם התפקודי.
בשלב הסמוי של עמילואידוזיס, כאשר ניתן לזהות הצטברות עמילואיד בכבד רק על ידי בדיקה מיקרוסקופית, הסימנים הראשונים של המחלה נעדרים. עם התפתחות נוספת וגירעון תפקודי גובר של האיבר, התסמינים מתקדמים.
הכבד מתעבה בהדרגה, גדל. שיטת המישוש יכולה להשתנות, אך גבולות האיבר חלקים וללא כאבים. לעיתים נדירות, הפתולוגיה מלווה בכאב באזור התת-צלעי בצד ימין, בעיות בעיכול, הגדלת הטחול, הצהבה של העור, הריריות והלומן, תסמונת דימומית.
התסמינים האופייניים ביותר לעמילואידוזיס בכבד: [ 9 ], [ 10 ]
- הצטברות עמילואיד בכבד גורמת להפטומגליה ב-33-92% מהחולים;
- צהבת קלה
- יתר לחץ דם פורטלי;
- כולסטזיס בינוני עד חמור.
מכיוון שעמילואידוזיס לעיתים רחוקות מאוד משפיעה על איבר אחד בלבד, בדרך כלל קיימות תסמינים נוספים:
- כאשר מתפתחת נזק לכליות תסמונת נפרוטית ויתר לחץ דם עורקי עם אי ספיקת כליות נוספת, בצקת, לפעמים טרומבוז בוורידים הכלייתיים, לויקוציטוריה, המטוריה, היפופרוטאינמיה, אזוטמיה וכן הלאה;
- כאשר הלב מושפע, מתפתח מצב הדומה לקרדיומיופתיה רסטריקטיבית (הפרעות קצב, קרדיומגליה, גירעון לבבי הולך וגובר, חולשה וקוצר נשימה, בצקת, בתדירות נמוכה יותר - הצטברות נוזלים בחלל הבטן והפלאורלי, דלקת קרום הלב);
- אם מערכת העיכול מושפעת, עלולות להופיע מקרוגלוסיה, חולשה ופריסטלטיקה של הוושט, בחילות וצרבת, עצירות או שלשולים וכו';
- כאשר הלבלב מושפע, קיימים תסמינים של דלקת לבלב כרונית;
- אם מעורב מנגנון השרירים והשלד, מתפתחת פוליארתריטיס סימטרית, תסמונת התעלה הקרפלית, מיופתיה, ואם מערכת העצבים מושפעת, נמצאים פולינוירופתיה, שיתוק, לחץ דם נמוך אורתוסטטי, הזעה מוגברת ודמנציה.
אם התגובה הפתולוגית מתפשטת לעור, מופיעים פלאקים רבים דמויי שעווה על הפנים, הצוואר וקפלי העור. תמונה אפשרית של נוירודרמטיטיס, קדחת קשקש אדומה וסקלרודרמה.
השילוב של נגעים עמילואידיים מרובים ומגוון התסמינים מקשים הרבה יותר על זיהוי עמילואידוזיס בכבד ודורשים אבחון מקיף ומלא.
טפסים
על פי הסיווג של ארגון הבריאות העולמי, נבדלים חמישה סוגים של עמילואידוזיס:
- AL (ראשוני);
- AA (משני);
- ATTR (מערכתית תורשתית וסנילית);
- Aβ2M (בחולים בהמודיאליזה);
- AIAPP (בחולים עם סוכרת שאינה תלויה באינסולין);
- AB (למחלת אלצהיימר);
- AANF (עמילואידוזיס פרוזדורים סנילי).
יש עמילואידוזיס מקומי של הכבד, אך לרוב מדובר בנגע מערכתי, שבו התהליך הפתולוגי כולל גם את הכליות, הלב, הטחול, מערכת העצבים, כמו גם איברים ורקמות אחרים.
סיבוכים ותוצאות
עמילואידוזיס סיסטמית מובילה בהדרגה להתפתחות של תהליכים פתולוגיים חריפים שיכולים, בתורם, להוביל למוות. בין הסיבוכים הנפוצים והמאיימים ביותר הם:
- פתולוגיות זיהומיות תכופות (חיידקיות, ויראליות), כולל דלקת ריאות, פיילונפריטיס, גלומרולונפריטיס;
- אי ספיקת כבד וכליות כרונית;
- אי ספיקת לב כרונית (עשויה להקדים אוטם שריר הלב);
- שבץ מוחי דימומי.
פקקת ורידית מתרחשת כתוצאה מהצטברות ושקיעת חלבונים על דפנות הווריד. חלל כלי הדם הפגועים מצטמצם, מתפתחת אי ספיקת איברים. עם הזמן, על רקע היפרפרוטאינמיה ארוכת טווח, כלי הדם עלול להיסגר לחלוטין. כל אחד מהסיבוכים עלול להוביל לתוצאה שלילית - מוות.
אבחון של עמילואידוזיס בכבד
אם יש חשד לעמילואידוזיס בכבד, אמצעי אבחון מבוצעים לאחר התייעצות חובה, הן עם גסטרואנטרולוג והן עם מטפל, והן עם ראומטולוג, קרדיולוג, דרמטולוגים, נוירולוג ואורולוג. חשוב לבצע הערכה מקיפה של נתוני האנמנזה והביטויים הקליניים, ולבצע אבחון מעבדתי ואינסטרומנטלי מקיף.
הבדיקות כוללות בהכרח בדיקת שתן ודם. בעמילואידוזיס בכבד, לעיתים קרובות נמצא שילוב של לויקוציטוריה עם פרוטאינוריה וצילינדרוריה, והיפופרוטאינמיה - עם היפרליפידמיה, אנמיה, היפונתרמיה והיפוקלצמיה, ספירת טסיות מופחתת. פרפרוטאינים מזוהים בשתן ובאלקטרופורזה בסרום.
אבחון אינסטרומנטלי כולל:
- א.ק.ג., אקו;
- אולטרסאונד בטן;
- צילומי רנטגן של הקיבה, הוושט;
- איריגוגרפיה, צילומי רנטגן של בריום;
- אנדוסקופיה.
ממצאים רדיולוגיים של עמילואידוזיס בכבד כוללים הפטומגליה לא ספציפית, עלייה באקוגניות באולטרסאונד או צפיפות בטומוגרפיה ממוחשבת (CT), ועוצמת אות T1 מוגברת בהדמיית תהודה מגנטית (MRI). [ 12 ] סינטיגרפיה עם אינדיקטורים הקשורים ל-Tc-99m מראה ספיגה הטרוגנית, אך היא לא ספציפית. [ 13 ], [ 14 ] GC הוכח כמגביר את נוקשות הכבד כפי שנמדדה על ידי אלסטוגרפיה; [ 15 ], [ 16 ], [ 17 ] אך ישנם מעט דיווחי מקרים. אלסטוגרפיה בתהודה מגנטית (MRE) היא כיום השיטה הלא פולשנית המדויקת ביותר לגילוי ושלב פיברוזיס בכבד, [ 18 ], [ 19 ] MRE שימושי לגילוי התקדמות, תגובה לטיפול וחיזוי פירוק כבד בחולים עם פיברוזיס בכבד. [ 20 ]
קשה לקבוע עמילואידוזיס של הכבד באולטרסאונד: נקבעת הגדלה של האיבר, כאשר ההפטומגליה הספציפית ביותר עולה על 15 ס"מ. תחת פיקוח האולטרסאונד, מבוצעת ביופסיה, שהופכת למדד מכריע לאבחון. באמצעות מחט מיוחדת, נלקחת כמות קטנה של רקמת כבד, לאחר מכן היא נצבעת בצבע מיוחד ונבדקת תחת מיקרוסקופ, המאפשר לראות ישירות את משקעי העמילואיד.
אבחנה סופית נעשית רק לאחר גילוי סיבי עמילואיד ברקמת הכבד ובאיברים אחרים. סוג העמילואידוזיס שנקבע גנטית נקבע על ידי בדיקה גנטית-רפואית מדוקדקת של אילן היוחסין.
אבחון דיפרנציאלי
יש לחשוד בעמילואידוזיס בכל החולים עם שילוב של פרוטאינוריה כלייתית, קרדיומיופתיה רסטריקטיבית, נוירופתיה אוטונומית או פריפרית והפטומיאליה, גם בהיעדר פאראפרוטאין חד שבטי. אימות סוג העמילואידוזיס חשוב מאוד מכיוון שהטיפול בנגעים בעלי אטיולוגיות שונות שונה מאוד.
אבחון היסטולוגי כרוך בצביעה באדום קונגו ולאחר מכן בדיקה מיקרוסקופית באור מקוטב. מומלץ לבצע ביופסיה של מספר דגימות רקמה בו זמנית. אם תוצאת הצביעה חיובית, מבוצעת ניתוח אימונוהיסטוכימי באמצעות נוגדנים חד שבטיים לחלבוני פרקורסור כדי לזהות את סוג העמילואיד.
ניתוח DNA מבוצע כדי להבדיל בין עמילואידוזיס ראשוני לבין וריאציות שונות של עמילואידוזיס שנקבעו גנטית. ניתן לבודד סיבי עמילואיד מדגימות ביופסיה ולבודד אותם לחומצות אמינו בודדות.
מחקרים נוספים לקביעת דיסקרסיה של תאי פלזמה:
- אלקטרופורזה של חלבוני סרום של דם ושתן;
- אימונו-אסאי לזיהוי שרשראות קלות חופשיות;
- אימונופיקסציה (אימונובלוטינג) של חלבוני סרום;
- שאיבת מח עצם וטרפנוביופסיה.
אבחון עמילואידוזיס בכבד הוא תהליך ארוך ועתיר עבודה, הדורש תשומת לב מוגברת של מומחים וציוד איכותי של מרפאות ומעבדות.
למי לפנות?
יַחַס של עמילואידוזיס בכבד
אמצעי הטיפול מכוונים להפחתת ריכוז חלבוני העמילואיד הקיימים בדם (ביטול הגורם לעמילואידוזיס) ולתמוך בתפקוד כבד תקין.
עמילואידוזיס משני דורש חסימת התהליך הדלקתי (בפתולוגיות זיהומיות כרוניות ואוטואימוניות). במחלות אוטואימוניות מומלץ להשתמש בציטוסטטיקה. כדי לחסל תהליכים זיהומיים כרוניים, אזור הדלקת מוסר לעיתים קרובות בניתוח. לעיתים קרובות גישה זו יכולה לעצור את התקדמותה של העמילואידוזיס ולשפר את תפקוד הכבד.
עמילואידוזיס ראשוני דורש שימוש בתרופות כימופרבטיביות ולעיתים השתלת מח עצם.
ההנחיות הנוכחיות ממליצות על שילוב של ציקלופוספמיד, בורטזומיב, דקסמתזון (CyBorD) ודארטומאב כטיפול קו ראשון בחולים שאובחנו לאחרונה עם AL.
בורטזומיב הוא מעכב פרוטאזום. פרוטאזומים מעורבים בהפחתת פרוטאוטוקסיות ובוויסות חלבונים השולטים בהתקדמות תאים ואפופטוזיס. תאי פלזמה המייצרים עמילואיד רגישים במיוחד לעיכוב פרוטאזום מכיוון שהם מסתמכים על הפרוטאזום כדי להפחית את ההשפעות הרעילות של שרשראות קלות ולמנוע אפופטוזיס.
דראטומומאב הוא נוגדן חד שבטי (mAb) הנקשר ל-CD38, גליקופרוטאין טרנסממברני המתבטא על פני תאי פלזמה, וגורם לאפופטוזיס. זוהי התרופה היחידה שאושרה במיוחד לטיפול בעמילואידוזיס של AL כאשר משתמשים בה בשילוב עם CyBorD. יעילות CyBorD-דראטומומאב גבוהה מאוד, כאשר 78% מהחולים השיגו תגובה המטולוגית משמעותית (מוגדרת כתגובה מלאה או תגובה חלקית טובה מאוד). חציון ההישרדות בקבוצה הקטנה של חולים שקיבלו CyBorD (n = 15) היה 655 ימים בהשוואה ל-178 ימים עבור חולים שקיבלו טיפול אחר מבוסס מלפלן-דקסמתזון (n = 10).
עם זאת, לטיפולים אלו תופעות לוואי רבות, כולל רעילות לבבית, מה שמוביל לצורך בהפחתת המינון או בהשעיית הטיפול, ושימוש באסטרטגיות טיפוליות אחרות, פחות יעילות אך נסבלות יותר.
איזטוקסימאב, נוגדן חד שבטי כנגד CD38 בדומה לדרטומאב, נחקר לטיפול בדיסקרזיה של תאי פלזמה העומדת בבסיס AL.
שלושה נוגדנים חד שבטיים, בירטמימאב, CAEL-101 ו-AT-03, נחקרים כעת להסרת סיבי עמילואיד מאיברים חולים. תוצאות המחקרים הללו יוכלו להציע ראיות ישירות להשערה כי על ידי הסרת סיבי שרשרת קלה מאיברים יש שיפור בתפקוד האיברים. [ 21 ]
על מנת לתמוך בתפקוד הכבד, נקבעות תרופות המבוססות על חומצה אורסו-דאוקסיכולית (לדוגמה - אורסוסן). חומצה אורסו-דאוקסיכולית מסייעת בייצוב קרומי התאים, מפחיתה את ההשפעה השלילית של חומצות שומן רעילות על קיפאון מרה הנגרם על ידי משקעי עמילואיד, ומסייעת בשיקום זרימת מרה תקינה.
בנוסף, טיפול סימפטומטי ותמיכה בתפקוד מבנים חיוניים אחרים כגון מערכת העצבים, הלב, הכליות וכו'. טיפול תומך לחולים עם עמילואידוזיס בכבד כולל היבטים קליניים שונים, כולל טיפול באי ספיקת לב, הפרעות קצב, הפרעות הולכה, תרומבואמבוליזם ונוכחות נלווית של היצרות אבי העורקים.
טיפולים אחרים תלויים בסוג העמילואידוזיס ובאילו חלקים בגוף מושפעים. טיפולים עשויים לכלול: [ 22 ]
- תרופות להקלה על תסמינים, כגון משככי כאבים, תרופות נגד בחילות או תרופות להפחתת נפיחות (משתנים);
- תרופות להפחתת עמילואיד;
- דיאליזה של כליות;
- השתלת כבד.
הכבד מייצר 95% מה-TTR (טרנסתירטין, חלבון המעורב בהובלת תירוקסין (T4) ובחלבון קושר רטינול. טרנסתירטין מסונתז בעיקר בכבד ועשיר בגדילי בטא הנוטים להצטבר לסיבים עמילואידיים בלתי מסיסים) הנמדדים בסרום. לכן, השתלת כבד הוצעה היסטורית (מאז 1990) כטיפול קו ראשון לחיסול המקור העיקרי של TTR עמילואידוגני בחולים עם הצורה המשפחתית (ATTRv), בעוד שהיא אינה מסומנת בצורת ATTR-wt. השתלת כבד של חולים צעירים בשלבים המוקדמים של המחלה קשורה לשיעור הישרדות גבוה של 20 שנה. השתלת כבד נראית יעילה יותר במוטציות מסוימות ופחות יעילה באחרות, כגון V122I (הקשורה לקרדיומיופתיה). השתלת כבד ולב משולבת אפשרית גם בחולי ATTRv צעירים עם קרדיומיופתיה, ונתוני ספרות על קבוצה קטנה של חולים מצביעים על כך שלשילוב זה יש פרוגנוזה טובה יותר מאשר השתלת לב בלבד.
חולים עם עמילואידוזיס בכבד אינם רשאים ליטול גליקוזידים לבביים ואנטגוניסטים של סידן כגון דילטיאזם או וראפמיל, אשר עלולים להצטבר בעמילואיד. מעכבי ACE וחוסמי בטא משמשים בזהירות.
בהיפוטנסיה אורתוסטטית, נקבעים מינרלוקורטיקואידים או גלוקוקורטיקואידים, תוך התחשבות בכך שהם עלולים לגרום לפירוק של אי ספיקת לב. גם המידודרין האלפא-אדרנומימטי (גוטרון) משמש בזהירות.
נוגדי פרכוסים ותרופות נוגדות דיכאון מתאימים בנוירופתיה.
במקרים מסוימים של עמילואידוזיס בכבד, רופאים צריכים לשקול השתלת איבר.
מְנִיעָה
בשל חוסר מידע על הפתוגנזה של עמילואידוזיס בכבד, מומחים אינם יכולים לפתח מניעה ספציפית של המחלה. לכן, המאמצים העיקריים מצטמצמים לגילוי וטיפול בזמן של כל פתולוגיה כרונית שיכולה לעורר את התפתחות ההפרעה. אם ישנם מקרים של עמילואידוזיס מכל לוקליזציה שהיא במשפחה, מומלץ לבקר באופן שיטתי אצל רופאים לבדיקות מרפאה.
באופן כללי, אמצעי מניעה מצטמצמים למיגור בזמן של מחלות זיהומיות, במיוחד אלו הנוטות להפוך לתהליך כרוני. מדובר במניעת התפתחות שחפת, זיהומים ריאתיים וכו'. חשוב לאבחן בזמן ולקבל טיפול הולם בזיהומים סטרפטוקוקליים, אשר יכולים להפוך לגורם לצורות כרוניות של תהליכים דלקתיים אוטואימוניים. אנו מדברים על סקרלטינה, דלקת שקדים סטרפטוקוקלית וכו'.
אם לחולה כבר יש מחלה אוטואימונית, עליו להתייעץ באופן שיטתי עם רופא, לעקוב אחר פעילות הפתולוגיה, ליישם את התרופות הדרושות כפי שנקבע על ידי הרופא, ולהתאים את המינונים בהתאם לאינדיקציות.
תַחֲזִית
הפרוגנוזה לחולים עם עמילואידוזיס בכבד אינה טובה. המחלה מתגברת באיטיות אך ברציפות, מה שבסופו של דבר גורם לתפקוד לקוי של האיברים הפגועים ולתוצאה קטלנית - בפרט, עקב אי ספיקת איברים.
חולים עם פתולוגיה סיסטמית מתים בעיקר כתוצאה מהתפתחות אי ספיקת כליות כרונית, אם כי במקרים מסוימים המודיאליזה או דיאליזה פריטונאלית אמבולטורית רציפה משפרת את הפרוגנוזה של חולים כאלה. ניתן להשוות את שיעור ההישרדות של חולים בהמודיאליזה, ללא קשר לסוגה, לאנשים עם פתולוגיות סיסטמיות אחרות וסוכרת.
הסיבה העיקרית למוות במהלך המודיאליזה היא התפתחות סיבוכים ממערכת הלב וכלי הדם.
השתלת כבד נחשבת זה מכבר לאחת משיטות הטיפול העיקריות במחלה, ושיעורי ההישרדות האופטימיים ביותר נצפים בחולים שגילם אינו עולה על 50 שנה (בתנאי שהתהליך הפתולוגי קצר מועד ומדד מסת הגוף תקין). לחולים עם עמילואידוזיס בכבד בשילוב עם נוירופתיה פריפרית יש פרוגנוזה גרועה במקצת.

