המומחה הרפואי של המאמר
פרסומים חדשים
HPV מסוג 33: תסמינים, טיפול
סקירה אחרונה: 04.07.2025

כל תוכן iLive נבדק מבחינה רפואית או נבדק למעשה כדי להבטיח דיוק עובדתי רב ככל האפשר.
יש לנו קווים מנחים קפדניים המקור רק קישור לאתרים מדיה מכובד, מוסדות מחקר אקדמי, בכל עת אפשרי, עמיתים מבחינה רפואית מחקרים. שים לב שהמספרים בסוגריים ([1], [2] וכו ') הם קישורים הניתנים ללחיצה למחקרים אלה.
אם אתה סבור שתוכן כלשהו שלנו אינו מדויק, לא עדכני או מפוקפק אחרת, בחר אותו ולחץ על Ctrl + Enter.
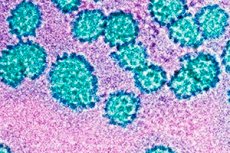
כיום, ברפואה, מופיעות יותר ויותר אבחנות שונות וקיצורים בלתי מובנים, אשר רק מפחידים אדם פשוט וחסר השכלה. דוגמה בולטת היא האבחנה של "HPV מסוג 33". מהי האבחנה המוזרה הזו? בואו נבחן את כל הפרטים ביתר פירוט.
מה זה?
אנשים רבים צריכים לעבור בדיקות מעבדה. לאחר קבלת התוצאות, ניתן לקרוא אבחנה מפחידה שכזו בבדיקת הדם. הדבר הראשון שעולה בראש הוא מה זה? מתברר שבמילים אחרות, קיצור זה יכול להיקרא וירוס הפפילומה האנושי. קוד הזן מצוין לידו - 33. זהו וירוס שלעתים קרובות נותר אצל נציגי הגזע הקווקזי.
נגיף הפפילומה האנושי (HPV) 33, חבר בקבוצת אלפא-9, מהווה כ-5% ממקרי סרטן צוואר הרחם ברחבי העולם.[ 1 ],[ 2 ]
מבנה HPV מסוג 33
מבנה הנגיף הוא ספציפי מאוד. ראשית, יש לציין שגודל הנגיף יכול לנוע בטווח רחב למדי - בין 100 ל-200 ננומטר. הממברנה מיוצגת על ידי שתי שכבות. השכבה הראשונה נוצרת על ידי ליפידים, השנייה מיוצגת על ידי קומפלקס של גליקופרוטאינים. הרכיבים מחוברים זה לזה באמצעות קשרים לא קוולנטיים.
גנוטיפים של HPV בסיכון גבוה 33
נגיף הפפילומה שייך למשפחת הפפילומה-וירוסים. זוהי קבוצה גדולה של נגיפים הגורמים לגידולים.
זוהו עשרים ושמונה וריאנטים של HPV33, אשר יצרו חמש קבוצות פילוגנטיות: שושלות A1, A2 ו-B (תת-קבוצות) שזוהו בעבר ושושלות חדשות A3 ו-C (תת-קבוצות).
גרסאות HPV33 סווגו לשתי שושלות עיקריות, A ו-B. שושלת A חולקה עוד לשתי תת-שושלות, A1, הכוללת את רצף האב-טיפוס [M12732.1 (Cole and Streeck, 1986) [ 3 ], ו-A2. סיווג זה מבוסס על הקביעה שרצף הגנום המלא של שושלת וריאנט עיקרית שונה בכ-1.0% משושלת וריאנט אחרת מאותו סוג HPV, כאשר הבדלים של 0.5-0.9% מגדירים תת-שושלות (Chen et al., 2011). [ 4 ]
שושלות משנה A1 מפוזרות ברחבי העולם, אם כי התדירות היחסית משתנה לפי אזור. שושלות משנה A2 זוהו לעיתים רחוקות באפריקה ובדרום אמריקה, בעוד שושלת משנה B ספציפית לאפריקה. שושלות משנה C נמצאו רק בדגימות מאפריקה, ותושגות משנה A3 היו ספציפיות לאסיה/אוקיאניה, נתמך על ידי שני דיווחים נוספים מסין (Wu et al., 2009) [ 5 ] ויפן [מבוסס על E6 בלבד (Xin et al., 2001)]. [ 6 ] עם זאת, יש לקחת בחשבון את הנדירות שנצפתה של שושלות A3 ו-C בעת פירוש תוצאות אלו.
דנ"א HPV 33
המרכיב העיקרי הוא גנים של אונקוגן, הכוללים רכיבי חלבון. הם נושאים מידע שיכול לעורר צמיחת גידול. ה-DNA של HPV 33 נוצר על ידי שתי ספירלות. זה משפר את תכונות הנגיף. תפקיד חשוב ניתן גם לגנים תאיים רגולטוריים, המווסתים את התהליכים התאיים העיקריים וגורמי הטרנספורמציה.
מחזור החיים HPV מסוג 33
חייו של וירוס הם מחזוריים ומתרחשים בכמה שלבים.
בשלב הראשון, הנגיף נספג בקולטני תא המארח. תהליך זה אפשרי בשל נוכחות גליקופרוטאינים בקומפלקס הממברנה ובוויריונים עצמם.
השלב השני מאופיין בחדירה פעילה של הנגיף ישירות למבנה התא של הפונדקאי. זה מפעיל את המנגנונים העיקריים של אינטראקציה של הנגיף עם המטריצה התאית. ישנם מנגנוני אינטראקציה שונים.
בשלב השלישי, הנגיף נע ברחבי התא ויוצר בועות בהן הוא מוגן באופן זמני. נקודת ההובלה הסופית של הנגיף היא הגעה לריבוזומים ול-ER. לעיתים, חלקיקי הנגיף והנגיפים עצמם נודדים לגרעין התא.
ניתן לתאר את השלב הרביעי כתהליך של פירוק הווירוס. מהות תהליך זה היא דה-חלבון ושחרור מהסופר-קפסיד והקפסידים.
בשלב החמישי, הוויריון מתמוסס לחלוטין, ומתחיל תהליך הסינתזה של וירוסים, אשר לאחר מכן הורסים את התא ומשוחררים החוצה.
בשלב השישי, הויריון מורכב ונוצר הנוקלאוקפסיד. תהליך ההרכבה העצמית של חלקיקי הנגיף מתחיל.
בשלב השביעי, חלקיקי הנגיף עוזבים את התא. בהתאם לכך, מתחיל השלב הפעיל של הזיהום, התקדמותו.
לאחר מכן, מחזור החיים חוזר על עצמו, תאים חדשים מעורבים, ובהתאם, המחלה מתפתחת ומתקדמת.
פתוגנזה
HPV מועבר בעיקר באמצעות מגע עור לעור. מחקרים אפידמיולוגיים מצביעים בבירור על כך שהסיכון להידבק ב-HPV באיברי המין ובסרטן צוואר הרחם קשור לפעילות מינית. HPV עמיד מאוד לחום וייבוש, והעברה אל-מינית יכולה להתרחש גם, כמו באמצעות מגע ממושך עם בגדים מזוהמים משותפים [ 7 ]. אדם נמצא בסיכון גבוה יותר להידבק ב-HPV אם היו לו מספר פרטנרים מיניים בכל עת או שהוא בן זוג של מישהו שהיו לו מספר פרטנרים מיניים. פעילות מינית מוקדמת גם מעמידה את האדם בסיכון מוגבר, כמו גם היסטוריה של מחלות אחרות המועברות במגע מיני, יבלות באברי המין, בדיקות פאפ חריגות, או סרטן צוואר הרחם או הפין אצל האדם או בן זוג מיני. שימוש בקונדומים עלול לא להגן כראוי על אנשים מחשיפה ל-HPV מכיוון ש-HPV יכול להיות מועבר באמצעות מגע עם רקמה נגועה בשפתיים, שק האשכים או אנאלי שאינה מוגנת על ידי קונדום.
בנוסף לפעילות מינית, גיל הוא גורם סיכון חשוב לזיהום ב-HPV [ 8 ]. הפעילות המטאפלסטית הגבוהה ביותר נצפית במהלך גיל ההתבגרות וההריון הראשון ויורדת לאחר גיל המעבר. זיהום ב-HPV שכיח ביותר בקרב נשים צעירות פעילות מינית בגילאי 18 עד 30. השכיחות יורדת בחדות לאחר גיל 30. עם זאת, סרטן צוואר הרחם שכיח יותר בקרב נשים מעל גיל 35, דבר המצביע על זיהום בגיל צעיר יותר והתפתחות סרטן איטית.
התגובה החיסונית העיקרית לזיהום HPV היא בתיווך תאי; לכן, מצבים הפוגעים בחסינות התאית, כגון השתלת כליה או מחלות ויראליות בבני אדם, מגבירים את הסיכון להידבקות והתקדמות של HPV. [ 9 ], [ 10 ]
דיכוי חיסוני מקומי הנגרם מעישון ופעילות מוטגנית של רכיבי סיגריות הודגם בתאי צוואר הרחם ועשוי לקדם התמדה של HPV או טרנספורמציה ממאירה בדומה לזו שנצפתה בריאות. [ 11 ], [ 12 ] בסך הכל, ידיעת אופן המעבר של HPV 33 יכולה לסייע במניעת זיהום.
תסמינים
ישנן מספר צורות של המחלה. התסמינים תלויים בכך. בסוג המיני של המחלה, הריריות של איברי המין ומערכת הרבייה ניזוקות. מופיעים כאב, גירוד, צריבה וגירוי. לעתים קרובות, התסמינים דומים לקיכלי: מופיעה הפרשה לבנה, לפעמים גבינתית. יבלות, גידולים ופפילומות מופיעים לעתים קרובות ישירות על הרירית של הנרתיק, תעלת צוואר הרחם והרחם.
בצורה עורית, יבלות ופפילומות עשויות להופיע על העור. הן ממוקמות בעיקר בשכבה העליונה של העור - האפידרמיס. הן יכולות להיות שטוחות או מוגבהות. כמו כן, ראוי לציין כי יבלות יכולות לגדול ולהתרבות די מהר. הן יכולות להיות בודדות או מרובות. לעתים קרובות, יבלות הן צורת הביטוי היחידה של מחלה זו.
זיהום HPV המועבר במגע מיני גורם לאחת משלוש תוצאות אפשריות.
- הראשונה היא יבלות אנוגניטליות (קונדילומה אקומינטום) על או סביב איברי המין ופי הטבעת אצל גברים ונשים כאחד.
- התוצאה השנייה היא זיהום סמוי או לא פעיל, שבו מעט אנשים יודעים שהם נגועים מכיוון שתסמינים מורגשים מופיעים לעיתים רחוקות והאזור הנגוע נשאר תקין מבחינה ציטולוגית. DNA של HPV קיים בכ-10% מהנשים עם אפיתל צווארי תקין מבחינה ציטולוגית.
- התוצאה השלישית היא זיהום פעיל, המקושר לסוגי HPV בסיכון גבוה, שבהם הנגיף גורם לשינויים בתאים נגועים שיכולים להוביל לנאופלזיה תוך-אפיתליאלית של הפין, השופכה, הנרתיק, הפות או צוואר הרחם. סוגי HPV בסיכון גבוה כוללים סוגים הקשורים לסרטן צוואר הרחם וסוגים המוגדרים כסיכון בינוני, המיוצגים בתדירות נמוכה יותר בסרטן. זיהומים אלה יכולים להוביל לסרטן צוואר הרחם. מחקרים פרוספקטיביים הראו כי 15 עד 28% מהנשים שהיו חיוביות ל-HPV DNA פיתחו SIL תוך שנתיים, בהשוואה ל-1 עד 3% בלבד מהנשים שהיו שליליות ל-HPV DNA.
פפילומות
זה נראה כמו יבלת, או גוש קטן שעולה על גבעול. מבנה זה מיוצג על ידי רקמת חיבור. הוא מכוסה באפיתל רב שכבתי בחלקו העליון. הוא יכול להתרומם חזק למדי מעל פני השטח (על גבעול) עליו הוא גדל, ויכול גם להיות שטוח ולהתפשט אופקית.
קצב הגדילה נמוך למדי, והוא קשור לגידולים בעלי צמיחה איטית. הסכנה נגרמת על ידי גידולים הממוקמים על איברים פנימיים: הם עלולים להינזק ולגרום לדימום. כאשר הם ממוקמים בלומן של איברים פנימיים (גרון, ושט, מעיים), הם עלולים לגדול ולסגור את החלמן. זה גורם לפתולוגיות המתאימות: חנק, חסימה. יש להסיר גידולים כאלה. השיטה העיקרית לטיפול בפפילומה היא כירורגית, הכוללת כריתה.
HPV 33 אצל גברים
לעתים קרובות גברים נשאים של נגיף זה, אך המחלה אינה מתבטאת בהם. הנגיף יכול להישאר בדם בצורה לא פעילה, או פשוט להיות מדוכא על ידי מערכת החיסון. אך במגע עם אישה, היא נדבקת לעיתים קרובות, מכיוון שלנשים יש חסינות נמוכה בהרבה, והיא אינה מאפשרת להן להתנגד באופן מלא לזיהום.
הביטוי העיקרי הוא היווצרות פפילומות (מרובות, בודדות). לצורך טיפול ב-HPV 33 אצל גברים, משתמשים בתרופות, צמחי מרפא ותכשירים הומאופתיים.
HPV 33 אצל נשים
נשים סובלות מנגיף זה לעתים קרובות יותר. במקרה זה, הצורה הגניטלית של המחלה שולטת. לרוב, היא מתבטאת בצורת פפילומות וקונדילומות הממוקמות על הקרום הרירי של איברי המין. הסכנה היא שקיימת אפשרות לניוון ממאיר של גידולים אלה, הפיכתם לגידול ממאיר. ראוי לציין שלעתים קרובות הדרך היחידה לטפל בהם היא כריתה כירורגית. אך לאחר מכן, נדרש טיפול נוסף, שמטרתו למנוע הישנות, מניעת גידולים חוזרים.
HPV 33 ודיספלזיה בינונית
מאפיין ייחודי הוא שהם בעלי פוטנציאל אונקוגני, כלומר, הם מעוררים התפתחות של גידולים ממאירים בתנאים מסוימים: חסינות מופחתת, תגובתיות ורגישות מוגברת, חולשה, ירידה בסיבולת ובעמידות של הגוף, שיבוש המחזור הביוכימי, מצב מבני ותפקודי תקין של הגוף, כמו גם חוסר איזון הורמונלי. בתנאים כאלה, מתפתחות פפילומות, פיברומות, מיומות, פיברומיומות, גידולים סיביים. זוהי דיספלזיה בינונית, הקשורה ישירות ל-HPV 33. ניתן לאפיין מצב זה כקדם לסרטן. תמיד קיים סיכון פוטנציאלי להתקדמות של מצבים אלה ולמעבר שלהם לגידולים ממאירים - סרקומות, סרטן, לוקמיה.
HPV 33 והריון
הופעת HPV 33 במהלך ההריון היא סימן רע, שכן נגיף זה יכול להוביל לפתולוגיות הריון. אלה יכולות להיות הפלות ספונטניות, הפלות, לידות מוקדמות או לידות מתות. לילדים יש לעיתים קרובות פגמים התפתחותיים: עיוותים פיזיים, סטיות שכליות ותפקודיות שונות, כמו גם פיגור שכלי, פיגור שכלי, פגמי דיבור והתפתחות רגשית.
אבל אלה מקרים קיצוניים המתרחשים עם ריכוז גבוה של וירוסים, עומס ויראלי גבוה. אחרת, עם טיפול ומעקב מתמיד של רופא, ההריון יכול להתקדם כרגיל. אבל תמיד קיים סיכון לפתח זיהום בדרכי השתן, דימום, שמתעצם במיוחד במהלך הלידה. קיים סיכון מוגבר לזיהום של הילד במהלך הלידה.
אבחון
תזדקק לוירולוג או אימונולוג מנוסה. ניתן גם לפנות למומחה למחלות זיהומיות, רופא מעבדה, ביוכימאי, בקטריולוג. אם במרפאה אין מומחים כאלה, עליך לפנות למטפל המיועד לאזור, והוא יפנה אותך למומחה המתאים, או פשוט יקבע את הבדיקות הנדרשות. השיטה העיקרית לאישור האבחנה היא אישור ישיר של נוכחות הנגיף בדם, שניתן להשיג רק על ידי ביצוע הבדיקות המתאימות. נעשה שימוש בשיטות מעבדה (אלה הן שיטות המחקר היעילות והאמינות היחידות).
ברוב המקרים, חומר המחקר הוא דם. נקבעו שיטות מחקר וירולוגיות וסרולוגיות, המאפשרות לזהות את הנגיף עצמו בדם, תוצרי פעילותו החיונית או DNA (שבריו). המעבדה משתמשת בשיטות ניתוח שונות. אך כדי לזהות את הנגיף, כדאי להשתמש בשיטת PCR, או ריצוף DNA, שבעזרתה מתגלים הנגיפים עצמם בדם, ולא נוגדנים כתגובה של מערכת החיסון לחדירת הנגיף.
מבחני PCR ספציפיים לסוג מבוססים על וריאציות רצף הקיימות בגנים E6 ו-E7 של תת-סוגי HPV. ארבעה עשר מבחני PCR ספציפיים לסוג עבור סוגי HPV בסיכון גבוה (HPV-16, -18, -31, -33, -35, -39, -45, -51, -52, -56, -58, -59, -66 ו- -68) מכוונים לכ-100 בסיסים בתוך ORF E7. [ 13 ]
הגנום מורכב ממעל 100,000 נוקלאוטידים, 9 גנים. על המשטח הפנימי ישנה מסגרת מטריצה. היא נוצרת על ידי חלבונים p17/18. הגנום נוצר על ידי 3 גנים מבניים ו-6 גנים רגולטוריים. כמו כן, ראוי לציין כי הנגיף משתנה למדי, במיוחד בהשוואה לנגיפים אחרים. מספר חוקרים עדיין עובדים על פענוח ה-DNA של HPV מסוג 33.
שיטת ELISA (בדיקת אנזים-קשור אימונוסורבנט) אינה אינפורמטיבית, מכיוון שהיא מגיבה לכמות קומפלקס האנטיגן-נוגדן. יתר על כן, נוגדנים נמשכים לאורך כל החיים לאחר מחלה אחת. לכן, לא ניתן להסיק מסקנה לגבי שלב ומידת הפעילות של הזיהום הנגיפי בגוף.
בדיקת רופא חשובה גם כן. הוא יבצע בדיקה מקיפה ויקבע אבחנה. במהלך בדיקה ויזואלית, הרופא כבר יוכל לחשוד בנוכחות HPV מסוג 33, שכן הוא מתבטא בסימנים ספציפיים. אך כדי לאשר סופית את המחלה, חשוב לא רק לאבחן אותה, אלא לבצע אבחנה מבדלת. משמעות הדבר היא שיש להבדיל את התסמינים ממקרים דומים אחרים וביטויים דומים.
שיטות נוספות עשויות לכלול בדיקה מיקרוסקופית, גירוד. בהתאם לחומרת הפתולוגיה, ייתכן שיידרש אימונוגרם, בדיקות דם ושתן קליניות וביוכימיות, ובדיקות דיסבקטריוזיס.
מיקרוסקופיה תסייע בזיהוי הנגיף עצמו או תוצרי הפסולת שלו במריחה, לבחון את המאפיינים והמאפיינים הספציפיים תחת מיקרוסקופ. בהתבסס על נתונים אלה, ניתן לקבוע את המיקום השיטתי הברור של הפתוגן, עד למין ולסוג. ככל שזיהוי כזה יבוצע בצורה מדויקת יותר, כך ניתן יהיה לבחור טיפול בצורה מדויקת ויעילה יותר. חשוב גם לקבל אינדיקטורים כמותיים, שכן תוכנית הטיפול הנוסף ויעילותו תלויות בכמות הנגיף בדם (עומס ויראלי).
השיטה העיקרית לגילוי HPV בסיכון גבוה נותרה משטח פאפ (PAP). בדיקה זו נקראה על שם הפתולוג ג'ורג' פאפניקולאו, שהציג את הבדיקה בשנת 1949 לפני שהגורם לסרטן צוואר הרחם היה ידוע. מאז הצגתה, משטח הפאפ סייע להפחית את שכיחות סרטן צוואר הרחם ואת שיעורי התמותה בכמחצית עד שני שלישים. [ 14 ] משטח הפאפ הוא כלי סינון המחפש שינויים בתאי אזור הטרנספורמציה של צוואר הרחם. לעתים קרובות, שינויים אלה נגרמים על ידי HPV.
HPV נורמה 33
מנקודת מבט רפואית וביולוגית, הנורמה נחשבת להיעדר מוחלט של וירוסים בדם. אך זהו מקרה אידיאלי, שהוא נדיר ביותר בתנאי החיים המודרניים. לכן, ישנן נורמות מותנות מסוימות של HPV 33 בגוף. אך הן שונות מאוד במדינות שונות. ישנן רק מדינות מעטות בהן היעדר מוחלט של הנגיף בדם נחשב לנורמה.
טיפול
הטיפול מורכב בעיקר מכריתה כירורגית של גידולים. כיום, בנוסף לניתוח המסורתי, קיימות מספר רב של שיטות להסרת פפילומות. לפיכך, השיטות היעילות ביותר הן הסרת פפילומות בלייזר, קריותרפיה, גלי רדיו ותדרי רדיו, אלקטרוקואגולציה, תרמית ואלקטרותרמית של הסרה של פפילומות. ישנה גם הסרה של פפילומות באמצעות כימיקלים.
רוב השינויים בתאי צוואר הרחם הנגרמים על ידי HPV הם חולפים, ו-90% מהם נסוגים באופן ספונטני תוך 12-36 חודשים כאשר מערכת החיסון מסלקת את הנגיף.[ 15 ]
באופן מסורתי, נעשה שימוש בטיפול אנטי-ויראלי. לדוגמה, תרופות מסורתיות כוללות אינוסיפלקס, אינטרפרון, אמיקסין, ציקלופרון, פודופילין. פודופילין, חומר ציטוטוקסי שעוצר מיטוזה במטאפאזה (משמש גם לטיפול ביבלות באברי המין), בשילוב עם וידראבין, מעכב DNA פולימראז המדכא ביטוי גנים של HPV וצמיחת תאים בקווי תאי סרטן צוואר הרחם. [ 16 ]
IFN ו-5-פלואורורציל תוך-נרתיקי הראו תגובות משתנות במחקרים קליניים ובמחקרים במבחנה. IFN-α מאושר לטיפול ביבלות באברי המין. השפעותיהם של IFN-α, IFN-β ו-IFN-γ נחקרו במספר שורות תאי קרצינומה אנושיים.[ 17 ]
חשוב לבצע טיפול אימונומודולטורי שמטרתו לנרמל את מצב החסינות. בדרך כלל נדרש טיפול אימונוסטימולטורי, המבוסס על הגברת החסינות. כתוצאה מכך, מערכת החיסון מתנגדת באופן עצמאי לזיהום, עמידותה וסיבולתה גוברים, והנגיף מדוכא.
טיפול מסורתי משמש למניעה, להחלמה לאחר הניתוח, או פשוט כאמצעי יעיל להפחתת מספר המיקרופלורה והעומס הנגיפי. זה יכול להיות טיפול תרופתי, אמצעים פיזיותרפיים שונים, רפואה מסורתית, הומאופתיה ופיטותרפיה. חיסונים אנטי-ויראליים מונעים מבוצעים גם כן, המסייעים במניעת ניוון ממאיר של תאים. כאשר נוצרות קונדילומות ופפילומות, משתמשים לעתים קרובות בצריבתן ובצריבתן.
מה לעשות אם מתגלה HPV 33?
ראשית, עליך לפנות לרופא שיבחר את הטיפול המתאים. ככל שהטיפול יתחיל מוקדם יותר, כך הוא יהיה יעיל יותר. הרופא, בהתבסס על תוצאות בדיקות מעבדה ובדיקות אינסטרומנטליות, יגיד לך מה לעשות. אם מתגלה HPV 33, ייתכן שיידרש טיפול תרופתי או כירורגי (כריתת הפפילומה). טיפול אנטי-ויראלי, אימונוסטימולטורי משמש גם כן.
האם ניתן לרפא HPV 33?
פתולוגיה זו מגיבה היטב לטיפול אם מערכת החיסון תקינה. לכן, אם מערכת החיסון חלשה, ניתן לראות החמרות, מחלות והישנות שונות. הסכנה היא שהנגיף עלול להיות אונקוגני. אם מערכת החיסון תקינה, הנגיף יכול פשוט להישאר בדם מבלי לגרום להחמרה של הזיהום.
לכן, בתשובה לשאלה: "האם ניתן לרפא HPV 33", אי אפשר לתת תשובה ברורה. לכן, חשוב לשמור על חסינות ברמה תקינה. הימנעו מעבודה יתרה, לחץ. בעת ביצוע טיפול אנטי-ויראלי, גירוי מערכת החיסון, טיפול בוויטמינים, ניתן להעביר את הנגיף למצב לא פעיל. לאחר מכן הוא יישאר בדם מבלי לגרום למחלה חריפה. אבל כמעט בלתי אפשרי לחסל לחלוטין את הנגיף מהדם, אדם נשאר נשא של הנגיף ויכול להדביק אחרים.
מניעה HPV מסוג 33
מניעה מבוססת על הקפדה על כללי היגיינה, קיום חיי מין נאותים (בן זוג קבוע, שימוש באמצעי הגנה במגע עם בני זוג זמניים, טיפול מונע אם לבן הזוג המיני יש זיהום. אלו הם אמצעי המניעה העיקריים והבסיסיים. חשוב גם לשמור על מערכת חיסונית תקינה - להתייעץ מעת לעת עם אימונולוג, להיבדק לנגיפים, זיהומים סמויים, ליטול קורסים של ויטמינים, ובמידת הצורך, גם ממריצים חיסוניים.
חשוב לאכול נכון, לכלול את הכמות הנדרשת של ויטמינים ומינרלים בתזונה, לעבור בדיקות מניעה סדירות, ובמידת הצורך, לעבור טיפול בזמן. שמירה על רמת חסינות גבוהה חשובה במיוחד, שכן התפתחות המחלה אפשרית רק עם חסינות מופחתת ומיקרופלורה לקויה.
הגישות העיקריות למניעת זיהום ב-HPV כוללות הן הפחתת סיכונים והן פיתוח חיסוני HPV. השימוש בקונדומים לטקס וקוטלי זרע יכול להפחית את הסיכון לזיהום ב-HPV. עם זאת, קונדומים אינם אמינים לחלוטין מכיוון ש-HPV יכול להיות מועבר במגע עם חלקים אחרים בגוף, כגון השפתיים, שק האשכים או פי הטבעת, שאינם מוגנים על ידי קונדום.
נערך מחקר בטיחות ואימונוגניות פאזה I, כפול סמיות, אקראי, מבוקר פלצבו, באמצעות חיסון תת-יחידה המורכב מ-VLP שנוצר מחלבון הקפסיד L1 העיקרי כולו של זן HPV-16 114K [ 18 ]. החיסון נוצר על ידי החדרת גן הקפסיד L1 לווקטור בקולובירוס. לאחר מכן הגן בא לידי ביטוי בתאי חרקים Sf9 שעברו טרנספקציה. מינון אופטימלי של 50 מיקרוגרם של חיסון HPV-16 L1 VLP ניתן באמצעות הזרקה לשריר הדלתואיד לאחר 0, 1 ו-4 חודשים. החיסון יצר רמות גבוהות של נוגדנים מנטרלים ספציפיים לסוג החיסון ללא אדג'ובנט ונסבל היטב.
נכון לשנת 2017, Gardasil 9 ® הוא חיסון ה-HPV היחיד הזמין בארצות הברית. חיסוני HPV אחרים זמינים מחוץ לארצות הברית. Gardasil 9 מסייע במניעת הדבקה ב-4 סוגים של HPV (16, 18, 6 ו-11) וב-5 סוגים אחרים בסיכון גבוה: 31, 33, 45, 52 ו-58. יחד, סוגים אלה גורמים לכ-90% ממקרי סרטן צוואר הרחם.
המלצות האגודה האמריקאית לסרטן לשימוש בחיסון HPV.
- חיסון שגרתי נגד HPV לבנות ולבנים צריך להתחיל בגיל 11-12. סדרת החיסונים יכולה להתחיל כבר בגיל 9.
- חיסון נגד HPV מומלץ גם לנשים בגילאי 13 עד 26 ולגברים בגילאי 13 עד 21 שטרם התחילו את סדרת החיסונים או שהתחילו אך לא סיימו את הסדרה. ניתן גם לחסן גברים בגילאי 22 עד 26.
- חיסון HPV מומלץ גם בגיל 26 לגברים המקיימים יחסי מין עם גברים ולאנשים עם מערכת חיסונית מוחלשת (כולל אנשים עם זיהום HIV) אם לא חוסנו בעבר.
- עבור אנשים בגילאי 22 עד 26 שטרם התחילו את החיסונים או שהתחילו אך לא סיימו את הסדרה, חשוב לדעת שחיסון בגילאים מבוגרים פחות יעיל בהפחתת הסיכון לסרטן.
תַחֲזִית
ברוב המקרים, עם טיפול נכון ובזמן, הפרוגנוזה תהיה חיובית. נגיף HPV מסוג 33 קל למדי לחסל, העיקר הוא לשמור על חסינות תקינה, לפעול לפי כל המלצות הרופא. אם מופיעות פפילומות, ייתכן שיהיה צורך בהסרתן כירורגית (כריתה). זהו הליך מהיר וללא כאבים שכמעט ואינו דורש החלמה. טיפול אנטי-ויראלי ממלא תפקיד חשוב. אם לא מטופל, עלולים להיווצר סיבוכים. המסוכן ביותר הוא התפתחות של גידולים ממאירים.

