מערכת מתן תרופות בלולאה סגורה יכולה לשפר את הכימותרפיה
סקירה אחרונה: 14.06.2024

כל תוכן iLive נבדק מבחינה רפואית או נבדק למעשה כדי להבטיח דיוק עובדתי רב ככל האפשר.
יש לנו קווים מנחים קפדניים המקור רק קישור לאתרים מדיה מכובד, מוסדות מחקר אקדמי, בכל עת אפשרי, עמיתים מבחינה רפואית מחקרים. שים לב שהמספרים בסוגריים ([1], [2] וכו ') הם קישורים הניתנים ללחיצה למחקרים אלה.
אם אתה סבור שתוכן כלשהו שלנו אינו מדויק, לא עדכני או מפוקפק אחרת, בחר אותו ולחץ על Ctrl + Enter.
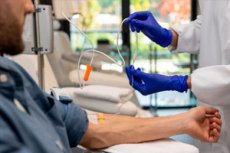
כאשר חולי סרטן עוברים כימותרפיה, המינונים של רוב התרופות מחושבים על סמך שטח גופו של המטופל. אינדיקטור זה מוערך באמצעות משוואה שבה מחליפים את הגובה והמשקל של המטופל. משוואה זו נוסחה בשנת 1916 על סמך נתונים של תשעה חולים בלבד.
גישה פשטנית זו למינון אינה לוקחת בחשבון גורמים אחרים ועלולה לגרום לכך שהמטופל יירשם ליותר מדי או מעט מדי מהתרופה. כתוצאה מכך, חלק מהמטופלים עלולים לחוות רעילות מוגזמת או חוסר יעילות מכימותרפיה.
כדי לשפר את הדיוק של מינון הכימותרפיה, מהנדסי MIT פיתחו גישה חלופית המאפשרת התאמה אישית של המינון לכל מטופל. המערכת שלהם מודדת את כמות התרופה בגוף המטופל, והנתונים האלה מוכנסים לבקר, שיכול להתאים את קצב העירוי בהתאם.
גישה זו עשויה לסייע בפיצוי על הבדלים בפרמקוקינטיקה של התרופות הנגרמים מהרכב הגוף, נטייה גנטית, רעילות איברים הנגרמת על ידי כימותרפיה, אינטראקציות עם תרופות ומזונות אחרים ותנודות יממה באנזימים האחראים לפירוק תרופות כימותרפיות, אומרים החוקרים.
"על ידי זיהוי ההתקדמות בהבנת האופן שבו תרופות עוברות חילוף חומרים ויישום כלים הנדסיים כדי לפשט מינון מותאם אישית, אנו מאמינים שאנו יכולים לעזור לשנות את הבטיחות והיעילות של תרופות רבות", אומר ג'ובאני טרברסו, עוזר פרופסור להנדסת מכונות ב-MIT ו גסטרואנטרולוג בבית החולים. Brigham and Women's Hospital ומחבר בכיר של המחקר.
לואיס דה רידר, סטודנט לתואר שני ב-MIT, הוא המחבר הראשי של המאמר שפורסם ב-Med.
ניטור רציף
במחקר זה, החוקרים התמקדו בתרופה בשם 5-fluorouracil, המשמשת לטיפול בסרטן המעי הגס וסוגים אחרים של סרטן. התרופה ניתנת בדרך כלל על פני תקופה של 46 שעות והמינון נקבע באמצעות נוסחה המבוססת על גובה ומשקל המטופל, המספקת אומדן של שטח הפנים של הגוף.
עם זאת, גישה זו אינה מתייחסת להבדלים בהרכב הגוף, אשר עשויים להשפיע על התפלגות התרופה בגוף, או שינויים גנטיים המשפיעים על חילוף החומרים שלה. הבדלים אלו יכולים להוביל לתופעות לוואי מזיקות אם יש יותר מדי מהתרופה. אם התרופה לא מספיקה, ייתכן שהיא לא תהרוג את הגידול כצפוי.
"אנשים עם אותו שטח גוף עשויים להיות בעלי גבהים ומשקלים שונים מאוד, מסת שריר שונה או גנטיקה שונה, אבל כל עוד הגובה והמשקל שמוכנסים למשוואה זו נותנים את אותו שטח גוף, המינון שלהם זהה." אומר DeRidder, מועמד לדוקטורט בתכנית להנדסה רפואית ופיזיקה רפואית בתכנית למדעי הבריאות והטכנולוגיה של הרווארד-MIT.
גורם נוסף שיכול לשנות את כמות התרופה בדם בכל זמן נתון הוא התנודה הצירקדית של אנזים הנקרא דיהידרופירימידין דהידרוגנאז (DPD), המפרק את 5-fluorouracil. הביטוי של DPD, כמו אנזימים רבים אחרים בגוף, מווסת על ידי קצב צירקדי. לפיכך, הפירוק של 5-FU DPD אינו קבוע, אלא משתנה בהתאם לשעה ביום. מקצבי יממה אלו יכולים לגרום לתנודות פי עשרה בכמות 5-fluorouracil בדם של המטופל במהלך עירוי.
"באמצעות שטח הפנים של הגוף לחישוב מינון הכימותרפיה, אנו יודעים שלשני אנשים יכולות להיות רעילות שונות לחלוטין מ-5-fluorouracil. למטופל אחד יכול להיות מחזורי טיפול עם רעילות מינימלית ולאחר מכן מחזור עם רעילות נוראית. משהו השתנה באופן זה כימותרפיה שעברה מטבוליזם של המטופל ממחזור אחד למשנהו שיטת המינון המיושנת שלנו אינה קולטת את השינויים הללו, והמטופלים סובלים כתוצאה מכך", אומר דאגלס רובינסון, אונקולוג קליני במכון לסרטן דנה-פרבר ומחבר המאמר.
אחת הדרכים לנסות לפצות על השונות בפרמקוקינטיקה של הכימותרפיה היא אסטרטגיה הנקראת ניטור תרופות טיפוליות, שבה המטופל מספק דגימת דם בתום מחזור טיפול אחד. לאחר ניתוח דגימה זו עבור ריכוזי תרופה, ניתן להתאים את המינון, במידת הצורך, בתחילת המחזור הבא (בדרך כלל לאחר שבועיים עבור 5-fluorouracil).
גישה זו הוכחה כמובילה לתוצאות טובות יותר עבור חולים, אך לא נעשה בה שימוש נרחב עבור כימותרפיות כגון 5-fluorouracil.
חוקרים MIT רצו לפתח סוג דומה של ניטור, אך בצורה אוטומטית שיכולה להתאים אישית את מינון התרופה בזמן אמת, מה שיכול להוביל לתוצאות טובות יותר עבור המטופלים.
במערכת הלולאה הסגורה שלהם, ניתן לעקוב באופן רציף אחר ריכוזי התרופות והמידע הזה משמש להתאמה אוטומטית של קצב עירוי התרופות הכימותרפי כדי לשמור על המינון בטווח היעד.
מערכת לולאה סגורה זו מאפשרת התאמה אישית של מינון התרופה כדי לקחת בחשבון מקצבים יממה של רמות משתנות של אנזימים המטבולים תרופות, כמו גם כל שינוי בפרמקוקינטיקה של המטופל מאז הטיפול האחרון, כגון רעילות איברים הנגרמת על ידי כימותרפיה.
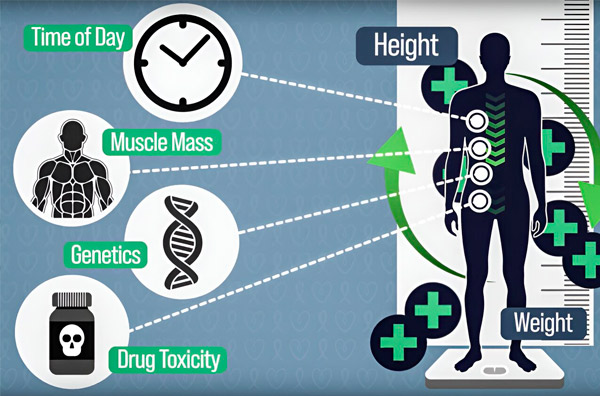
כדי לדייק את מינון הכימותרפיה, מהנדסי MIT פיתחו דרך למדוד באופן רציף את כמות התרופה בגוף המטופל במהלך עירוי בן שעות. זה יעזור לפצות על הבדלים הנגרמים על ידי הרכב הגוף, גנטיקה, רעילות תרופות ותנודות יממה. מקור: מסופק על ידי חוקרים.
המערכת החדשה שפותחה על ידי החוקרים, הידועה בשם CLAUDIA (Closed-Loop AUtomated Drug Infusion regulAtor), משתמשת בציוד זמין מסחרית לכל שלב. דגימות דם נלקחות כל חמש דקות ומוכנות במהירות לניתוח. הריכוז של 5-fluorouracil בדם נמדד ומשווה לטווח היעד.
ההבדל בין ריכוז המטרה והריכוז הנמדד מוכנס לאלגוריתם הבקרה, אשר לאחר מכן מתאים את קצב העירוי במידת הצורך כדי לשמור על המינון בטווח הריכוז שבו התרופה יעילה ואינה רעילה.
"פיתחנו מערכת שבה אנו יכולים למדוד באופן רציף את ריכוזי התרופות ולהתאים את קצב העירוי בהתאם כדי לשמור על ריכוזי התרופה בתוך החלון הטיפולי", אומר DeRidder.
התאמה מהירה
בניסויים בבעלי חיים, החוקרים מצאו כי באמצעות קלאודיה, הם הצליחו לשמור את כמות התרופה בגוף בטווח היעד של כ-45 אחוז מהזמן.
רמות התרופות בבעלי חיים שקיבלו כימותרפיה ללא CLAUDIA נותרו בטווח היעד רק 13 אחוז מהזמן בממוצע. במחקר זה, החוקרים לא בדקו את היעילות של רמות התרופה, אך מאמינים ששמירה על ריכוזים בתוך חלון היעד מביאה לתוצאות טובות יותר ולפחות רעילות.
CLAUDIA גם הצליחה לשמור על מינון 5-fluorouracil בטווח היעד גם כאשר ניתנה תרופה המעכבת את האנזים DPD. בבעלי חיים שטופלו במעכב זה ללא ניטור והתאמה מתמשכים, רמות 5-fluorouracil עלו עד פי שמונה.
להדגמה זו, החוקרים ביצעו ידנית כל שלב בתהליך באמצעות ציוד מדף, אך כעת מתכננים להפוך כל שלב לאוטומטי כך שניתן לבצע ניטור והתאמת מינון ללא התערבות אנושית.
כדי למדוד ריכוזי תרופות, החוקרים השתמשו בספקטרומטריית כרומטוגרפיה-מסה נוזלית בעלת ביצועים גבוהים (HPLC-MS), טכניקה שניתן להתאים לאיתור כמעט כל סוג של תרופה.
"אנו רואים עתיד בו נוכל להשתמש ב-CLAUDIA עבור כל תרופה בעלת תכונות פרמקוקינטיות מתאימות וניתנת לזיהוי באמצעות HPLC-MS, המאפשרת מינון מותאם אישית עבור תרופות רבות ושונות", אומר DeRidder.
