פרסומים חדשים
תקווה לתרופה ללישמניאזיס ויסצרלית קטלנית
סקירה אחרונה: 02.07.2025

כל תוכן iLive נבדק מבחינה רפואית או נבדק למעשה כדי להבטיח דיוק עובדתי רב ככל האפשר.
יש לנו קווים מנחים קפדניים המקור רק קישור לאתרים מדיה מכובד, מוסדות מחקר אקדמי, בכל עת אפשרי, עמיתים מבחינה רפואית מחקרים. שים לב שהמספרים בסוגריים ([1], [2] וכו ') הם קישורים הניתנים ללחיצה למחקרים אלה.
אם אתה סבור שתוכן כלשהו שלנו אינו מדויק, לא עדכני או מפוקפק אחרת, בחר אותו ולחץ על Ctrl + Enter.
התגלית של צוותו של סימון סטגר עשויה לסייע בפיתוח טיפול לצורה החמורה ביותר של לישמניאזיס. לישמניאזיס היא מחלה טרופית הפוגעת במספר גדל והולך של אנשים ברחבי העולם. בין 700,000 למיליון מקרים חדשים נרשמים מדי שנה. הגורם הסיבתי הוא טפיל פרוטוזואני מהסוג לישמניה, המועבר לבני אדם דרך עקיצת יתוש. לישמניאזיס כוללת שלוש צורות קליניות, שהצורה הבטנית היא החמורה ביותר.
אם לא מטופלת, לישמניאזיס ויסצרלית כמעט תמיד קטלנית. רוב המקרים מתרחשים בבנגלדש, ברזיל, אתיופיה, הודו, נפאל וסודן.
פרופסור סטגר מהמכון הלאומי למחקר מדעי (INRS) וצוותה, בשיתוף פעולה עם חוקרים אחרים מ-INRS ומאוניברסיטת מקגיל, הבחינו במנגנון חיסוני מפתיע הקשור ללישמניאזיס ויסצרלית כרונית. תגלית זו עשויה להיות צעד חשוב לקראת אסטרטגיה טיפולית חדשה למחלה זו. ממצאיהם פורסמו בכתב העת Cell Reports.
בזיהומים רבים, תאי T מסוג CD4 ממלאים תפקיד מפתח בהגנה של הפונדקאי. לרוע המזל, בזיהומים כרוניים כמו לישמניאזיס, שמירה על ספירת תאי CD4 תפקודית הופכת למשימה חשובה, שכן מערכת החיסון מופעלת ללא הרף כדי להגיב לפתוגן.
מגני מערכת החיסון החדשים עם זאת, מחקר שערכה פרופסור סטגר במעבדתה במרכז המחקר INRS ארמנד-פרפייר לביוטכנולוגיה ובריאות מצביע על כך שלתאים אלה עשויה להיות יותר מדרך אחת לשמור על קיומם.
"גילינו אוכלוסייה חדשה של תאי CD4 בעכברים שנדבקו בטפיל האחראי ללישמניאזיס ויסצרלית. לתאי T אלה יש תכונות מעניינות", אמר פרופסור סטגר.
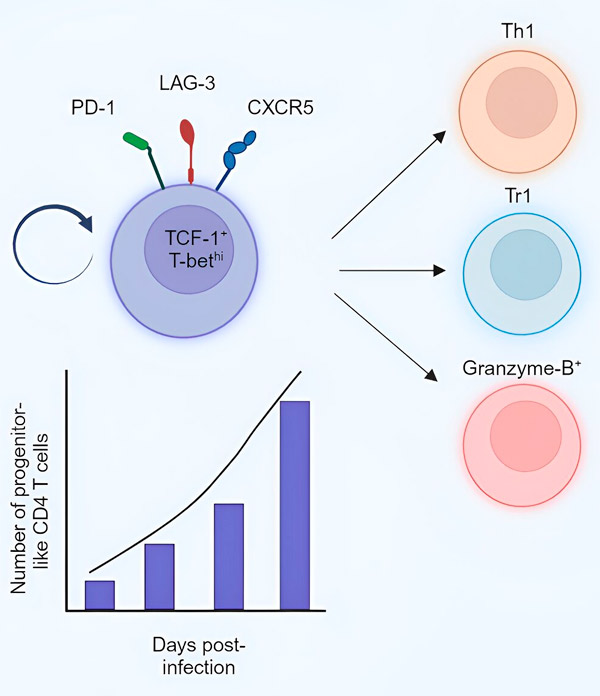
על ידי ניטור תאים חדשים אלה, המדענים שמו לב שמספרם גדל במהלך השלב הכרוני של המחלה, וכי בדומה לתאי אב, הם היו מסוגלים להתחדשות עצמית או להתמיין לתאי אפקטור אחרים האחראים לחיסול הטפיל או לתאים רגולטוריים המדכאים את תגובת המארח.
פרופסור סטגר מציין שתאי CD4 T בדרך כלל מתמיינים לתאי אפקטור מתאי CD4 T "נאיביים". אך במהלך זיהומים כרוניים, עקב הצורך המתמיד לייצר תאי אפקטור, תאי CD4 T נאיביים הופכים לעומסים יתר על המידה ויכולים להתדלדל.
"אנו מאמינים שבשלב הכרוני של לישמניאזיס ויסצרלית, האוכלוסייה החדשה שזיהינו אחראית על יצירת תאי אפקטור ותאי בקרה. זה יאפשר לפונדקאי למנוע את דלדול המאגר הקיים של תאי T CD4 נאיביים לאנטיגן מסוים", מסביר הדוקטורנט והמחבר הראשון של המחקר, שרדה סוומיניאתן.
אוכלוסיית הלימפוציטים החדשה שהתגלתה על ידי צוות INRS עשויה להפוך למחזק חיסוני מכריע, ולהחליף תאי CD4 T נאיביים עמוסים יתר על המידה.
"אם נוכל להבין כיצד לכוון את אוכלוסיית הלימפוציטים החדשה הזו להתמיין לתאי אפקטור הגנתיים, זה עשוי לעזור למארח להיפטר מטפיל הלישמניה", אמר פרופסור סטגר.
תרופה לזיהומים אחרים? המחקר מזכיר גם כי תאים דומים נמצאו בעכברים שנדבקו בנגיף לימפוציטי של כוריומנינגיטיס ובעכברים הנושאים את תולעת המעי H. polygyrus. לכן, ייתכן שאוכלוסייה זו קיימת בזיהומים כרוניים אחרים או בסביבות דלקתיות כרוניות אחרות.
עובדה זו פותחת סיכויים רחבים עוד יותר לתגלית שערך צוותו של פרופסור סטגר. "אם ההשערה שלנו נכונה, ניתן להשתמש בתאים אלה למטרות טיפוליות לא רק עבור לישמניאזיס ויסצרלית, אלא גם עבור זיהומים כרוניים אחרים", מסכם החוקר.
