פרסומים חדשים
יש שיטה חדשה לשיקום הראייה
סקירה אחרונה: 02.07.2025

כל תוכן iLive נבדק מבחינה רפואית או נבדק למעשה כדי להבטיח דיוק עובדתי רב ככל האפשר.
יש לנו קווים מנחים קפדניים המקור רק קישור לאתרים מדיה מכובד, מוסדות מחקר אקדמי, בכל עת אפשרי, עמיתים מבחינה רפואית מחקרים. שים לב שהמספרים בסוגריים ([1], [2] וכו ') הם קישורים הניתנים ללחיצה למחקרים אלה.
אם אתה סבור שתוכן כלשהו שלנו אינו מדויק, לא עדכני או מפוקפק אחרת, בחר אותו ולחץ על Ctrl + Enter.
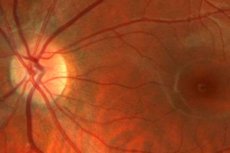
ביולוגים הצליחו להחדיר את הגן של חומר החלבון הרגיש לאור MCO1 לתאי עצב ברשתית של מכרסמים שאיבדו את ראייתם.
החוקרים החדירו גן לאובייקט ויראלי והחדירו אותו לאיברי הראייה של עכברים הסובלים מרטיניטיס פיגמנטוזה. חומר החלבון החדש לא עורר תגובה דלקתית, והמכרסמים עברו בהצלחה את הבדיקה הראייתית.
במהלך תפיסת התמונה הנראית לעין, קרני האור ממוקדות באזור הרשתית, המצויד בקולטני אור - הקונוסים והמוטות הידועים. הקולטנים מכילים חלבון רגיש לאור, אופסין, המגיב לזרימת הפוטונים וגורם ליצירת דחף עצבי תוך-קולטי. הדחף מועבר לתאי העצב הדו-קוטביים של הרשתית, ולאחר מכן הוא נשלח למוח.
אבל תוכנית כזו לא תמיד עובדת: אצל חולים עם רטיניטיס פיגמנטוזה (ישנם כ-1.5 מיליון כאלה בעולם), קולטני אור מאבדים את היכולת להגיב לאור, דבר הקשור לשינויים בגנים של אופסינים רגישים לאור. פתולוגיה תורשתית זו גורמת לירידה חזקה בתפקוד הראייה, עד לאובדן ראייה מוחלט.
טיפול תרופתי ברטיניטיס פיגמנטוזה הוא מורכב ואינו כרוך בשיקום, אלא רק בשימור היכולת התפקודית של הקולטנים "השורדים" הנותרים. לדוגמה, תכשירים של רטינול אצטט נמצאים בשימוש פעיל. ניתן לשקם את הראייה רק באמצעות התערבות כירורגית מורכבת ויקרה. עם זאת, שיטות אופטוגנטיות נכנסו לאחרונה ליישם: מומחים מטמיעים חומרי חלבון רגישים לאור ישירות בתאי העצב ברשתית, ולאחר מכן הם מתחילים להגיב לשטף האור. אך לפני המחקר הנוכחי, תגובה מתאים מהונדסים גנטית יכולה להתקבל רק לאחר אפקט אות חזק.
מדענים הכניסו חומר המגיב לאור יום לתאי עצב דו-קוטביים. נוצר מקטע DNA כדי להבליט אופסין, אשר לאחר מכן הוכנס לחלקיק ויראלי שאיבד את תכונותיו הפתוגניות: מטרתו הייתה להעביר ולארוז אותו למבנה גנטי. החלקיק הוזרק לעינו של מכרסם חולה: מקטע ה-DNA שולב בנוירונים של הרשתית. תחת שליטה מיקרוסקופית, מדענים שמו לב שהגנים הגיעו לגבול הפעילות שלהם עד השבוע הרביעי, ולאחר מכן הרמה התייצבה. כדי לבדוק את איכות הראייה לאחר ההליך, המכרסמים קיבלו משימה: למצוא אי יבש ומואר במים, בזמן שהם בחושך. הניסוי הראה כי ראיית העכברים השתפרה באופן משמעותי כבר בשבוע הרביעי-שמיני לאחר המניפולציה.
ייתכן בהחלט שהריפוי הגנטי שפותח ברשתית המכרסמים יותאם לטיפול בבני אדם לאחר סדרה של בדיקות נוספות. אם זה יקרה, לא יהיה צורך בהתערבויות כירורגיות יקרות, או בחיבור מכשירים מיוחדים להגברת אות האור. יידרש רק זריקה אחת או יותר של חומר חלבוני.
פרטים נוספים על המחקר ניתן למצוא בכתב העת Gene Therapy ובדף Nature
