פרסומים חדשים
חקירת מנגנון הופעת פריחות תרופות על העור
Last reviewed: 02.07.2025

כל תוכן iLive נבדק מבחינה רפואית או נבדק למעשה כדי להבטיח דיוק עובדתי רב ככל האפשר.
יש לנו קווים מנחים קפדניים המקור רק קישור לאתרים מדיה מכובד, מוסדות מחקר אקדמי, בכל עת אפשרי, עמיתים מבחינה רפואית מחקרים. שים לב שהמספרים בסוגריים ([1], [2] וכו ') הם קישורים הניתנים ללחיצה למחקרים אלה.
אם אתה סבור שתוכן כלשהו שלנו אינו מדויק, לא עדכני או מפוקפק אחרת, בחר אותו ולחץ על Ctrl + Enter.
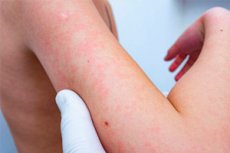
למרות שתרופות לעיתים קרובות עוזרות לחולים לרפא או להקל על מצבם, מיליוני אנשים ברחבי העולם סובלים מדי שנה מתגובות רעילות בלתי צפויות לתרופות. בפרט, פריחות כתוצאה מתרופות, הכוללות תסמינים כמו אדמומיות, שלפוחיות וגירוד בעור, הן די שכיחות.
תגובות חמורות לתרופות עלולות להיות מסכנות חיים ולהיות בעלות השלכות ארוכות טווח. לכן, הבנת האופן שבו ומדוע מתרחשות תגובות לתרופות היא תחום מחקר חשוב במדעי הרפואה.
לשם כך, מחקרים קודמים זיהו וריאנטים ספציפיים של גנים מסוימים כגורמים פוטנציאליים לפריחות כתוצאה מתרופות. מדענים מאמינים כי גנים המקודדים אנטיגן לויקוציטים אנושי (HLA), חלבון המתבטא על פני תאי דם לבנים הממלא תפקיד חשוב במערכת החיסון, מעורבים בהתפתחות פריחות כתוצאה מתרופות. עם זאת, תיאוריות עכשוויות אינן יכולות להסביר מדוע פריחות כתוצאה מתרופות הקשורות ל-HLA מתרחשות בדרך כלל על העור ולא באיברים מרובים בגוף.
כדי להתמודד עם פער הידע הזה, צוות מחקר שכלל את חברי הסגל שיגקי אאוקי, קוסיי איטו ואקירה קזאוקה מבית הספר למדעי הרפואה והרוקחות של אוניברסיטת צ'יבה ערך מחקר מעמיק על הקשר בין HLA לבין פריחות מתרופות. ממצאיהם פורסמו ב- PNAS Nexus.
החוקרים ערכו תחילה סדרה של ניסויים על קרטינוציטים של עכברים, שהם סוג התאים העיקרי הנמצא בעור. קרטינוציטים אלה שונו כדי לבטא גרסה ספציפית של גן HLA הנקרא HLA-B57:01, אשר נקשר באופן ספציפי לתרופה האנטי-ויראלית אבקביר. לאחר מכן הם אישרו את התוצאות הללו בעכברים מהונדסים גנטית המבטאים HLA-B 57:01 שנחשפו לאבקביר.
החוקרים מצאו כי קרטינוציטים המבטאים HLA-B*57:01 ונחשפו לאבקביר הציגו תגובות עקה של הרשת האנדופלזמית (ER) כגון שחרור מיידי של סידן לציטוזול וביטוי מוגבר של חלבון הלם חום 70 (HSP70). הם גם הבחינו בייצור מוגבר של ציטוקינים ובנדידת תאים חיסוניים. חשיפה לאבקביר גרמה לקיפול שגוי של HLA ב-ER, מה שהוביל לעקה ב-ER.
יתר על כן, החוקרים מצאו כי ניתן להפחית את הלחץ ב-ER באמצעות 4-פנילבוטיראט (4-PB). על ידי סילוק הלחץ הזה, הם הצליחו לדכא את הופעת תסמיני פריחה חמורים כתוצאה מסמים. ידע חדש זה עשוי לספק את הבסיס לאפשרויות טיפול חדשניות לפריחות כתוצאה מסמים.
אבל איך מידע חדש זה עומד בניגוד למה שכבר היה ידוע על HLA?
"מולקולות HLA הן מרכיב בלתי נפרד ממערכת החיסון שלנו, ובדרך כלל מציגות אנטיגנים זרים לתאי דם לבנים, אשר מעריכים את האנטיגנים הללו כעצמאיים או לא-עצמאיים. בתפקיד מבוסס זה, HLA ממלא בדרך כלל תפקיד משני", מסביר ד"ר אאוקי.
"עם זאת, המחקר שלנו מדגיש תפקיד חדש של מולקולת HLA בתאי עור. מצאנו שגנוטיפ HLA ספציפי בקרטינוציטים יכול לזהות תרופות מסוימות כזרות, מה שמעורר תגובת לחץ ברשת האנדופלזמית."
בסך הכל, תוצאות מחקר זה חושפות תפקיד חדש לחלבוני HLA בגילוי ותגובה לאיומים פוטנציאליים בתאי עור. תפקידיהם עשויים להרחיב הרבה מעבר להצגת אנטיגנים למערכת החיסון. יתר על כן, בהתחשב בכך שניתן לקבוע את וריאנט ה-HLA של אדם באמצעות בדיקות גנטיות, מחקר זה עשוי לסייע בפיתוח אמצעי מניעה ושיטות אבחון כנגד תגובות שליליות חמורות של תרופות.
לדברי ד"ר אאוקי, זה תואם את המגמות והכיוונים הנוכחיים במדע הרפואה. "בעוד 10 שנים, אנו מצפים להיכנס לעידן 'הגנום המקיף', שבו רפואה מותאמת אישית המבוססת על גנומים אינדיבידואליים תהפוך לנוהג סטנדרטי", הוא מעיר.
"בהתבסס על תוצאות מחקר זה, אנו מאמינים כי הבנה מקיפה של המנגנון העומד בבסיס תגובות לוואי תלויות HLA תאפשר טיפול רפואי בטוח, שיאפשר למטופלים להימנע מסבל מיותר עקב תופעות לוואי."
בסך הכל, מחקר עתידי בתחום זה עשוי למזער את התרחשות פריחות מתרופות ולהציל אנשים מתגובות שליליות שעלולות להיות קטלניות.
